题目内容
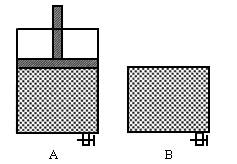
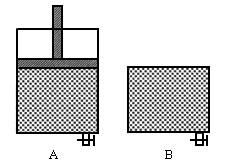
如图有两只密闭容器A和B,A容器有一个移动的活塞使容器内保持恒压,B容器能保持恒容,起始时向这两只容器中分别充入等量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等。在保持400℃的条件下使之发生如下反应:2SO2+O2ƒ2SO3,填写下列空格:
(1)达到平衡时所需的时间A容器比B容器________,A容器中SO2的转化率比B容器________。
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量氩气,A容器化学平衡________移动,B容器化学平衡________移动。
(3)达到(1)所述平衡时,若向两容器中通入等量的原反应气体,达到平衡时,A容器中SO3的体积分数比原平衡________,B容器中SO3的体积分数比原平衡________。
答案:
解析:
提示:
解析:
(1)短,大 (2)逆向,不 (3)相等,大
|
提示:
提示:(1)A、B原本状态相同,由于反应进行,混合气体物质的量减少,A中活塞下滑以保持恒压,而B中体积不变则压强减小,继续反应过程中,B是在小于A的压强条件下进行,所以v(A) >v(B),到达平衡的时间t(A) <t(B)。依照增大压强,平衡向该反应的正方向进行可知:A容器中SO2的转化率大于B容器中SO2的转化率。 (2)A中通入氩气,总压不变,活塞上移,对于反应气体相当于减压,平衡逆向移动,B容器中虽压强增大,但反应气体浓度未变,故平衡不移动。 (3)A中相当于两个等同状态的气态平衡体系混合,活塞自动上移,平衡不移动,各组分的体积分数不变;而B中加入SO2和O2这些反应物,相当于加压,平衡向正反应方向移动,SO3的体积分数增大。
|

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
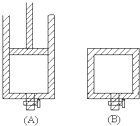 有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时间这两只容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等,如右图.在保持400℃的条件下使之发生如下反应:2SO2+O2?2SO3.
有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时间这两只容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等,如右图.在保持400℃的条件下使之发生如下反应:2SO2+O2?2SO3. 有两只密闭容器A和B,A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量SO3气体,并使A和B容积相等(如图所示)在保持400℃的条件下使之发生如下反应:2SO2+O2
有两只密闭容器A和B,A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量SO3气体,并使A和B容积相等(如图所示)在保持400℃的条件下使之发生如下反应:2SO2+O2  2SO3.则下列描述正确的是( )
2SO3.则下列描述正确的是( )