题目内容
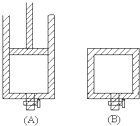 有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时间这两只容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等,如右图.在保持400℃的条件下使之发生如下反应:2SO2+O2?2SO3.
有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时间这两只容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等,如右图.在保持400℃的条件下使之发生如下反应:2SO2+O2?2SO3.请填写下列空白:
(1)到平衡时所需的时间A容器比B容器
少
少
(多、少),A容器中SO2的转化率比B容器中大
大
(大、小).(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量的He,
A容器中化学平衡
向左
向左
移动(向左、向右、不移动).B容器中化学平衡
不
不
移动(向左、向右、不移动).(3)达到(1)所述平衡后,若向两容器中再通入等量的原反应气体,达到平衡时,A容器中SO3的百分含量
不变
不变
.B容器中SO3的百分含量增大
增大
.(增大、减小、不变.)分析:(1)根据化学反应速率越快,到达平衡的时间越短;利用等效平衡来判断平衡移动来解答;
(2)根据容器中的压强对化学平衡的影响;
(3)根据浓度对化学平衡的影响,求出平衡移动后SO3的体积分数.
(2)根据容器中的压强对化学平衡的影响;
(3)根据浓度对化学平衡的影响,求出平衡移动后SO3的体积分数.
解答:解:(1)因A容器保持恒压,反应过程中体积变小,浓度增大,根据浓度越大,化学反应速率越快,到达平衡的时间越短,所以达到平衡所需时间A比B少,若A容器保持恒容,两容器建立的平衡等效,而实际上A容器体积减少,压强增大,平衡向正反应方向移动,所以A中SO2的转化率比B大,故答案为:少;大;
(2)平衡后,若向两容器通入数量不多的等量He,A容器体积增大,压强不变,参加反应的气体产生的压强减少,平衡向左反应方向移动,而B容器体积不变,浓度不变,平衡不移动,故答案为:向左;不;
(3)向两容器中通入等量的原反应气体,达到平衡后,A中建立的平衡与原平衡等效,所以SO3的体积分数不变,B容器中建立的平衡相当于在原平衡的基础上增大压强,平衡正向移动,B容器中SO3的体积分数增大,故答案为:不变;增大.
(2)平衡后,若向两容器通入数量不多的等量He,A容器体积增大,压强不变,参加反应的气体产生的压强减少,平衡向左反应方向移动,而B容器体积不变,浓度不变,平衡不移动,故答案为:向左;不;
(3)向两容器中通入等量的原反应气体,达到平衡后,A中建立的平衡与原平衡等效,所以SO3的体积分数不变,B容器中建立的平衡相当于在原平衡的基础上增大压强,平衡正向移动,B容器中SO3的体积分数增大,故答案为:不变;增大.
点评:本题考查化学平衡移动的判断,题目难度较大,注意等效平衡的理解和应用,明确浓度不变反应速率不变,则平衡不移动.

练习册系列答案
相关题目
 有两只密闭容器A和B,A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量SO3气体,并使A和B容积相等(如图所示)在保持400℃的条件下使之发生如下反应:2SO2+O2
有两只密闭容器A和B,A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量SO3气体,并使A和B容积相等(如图所示)在保持400℃的条件下使之发生如下反应:2SO2+O2  2SO3.则下列描述正确的是( )
2SO3.则下列描述正确的是( )
 SO3+ V2O4
SO3+ V2O4 2SO2+O2
在550 ℃时的平衡常数K= 。
2SO2+O2
在550 ℃时的平衡常数K= 。
 2SO3,有两只密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等物质的量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等(如下图所示)。
2SO3,有两只密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等物质的量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等(如下图所示)。
 3H2(g)+N2(g),并达到平衡。则:
3H2(g)+N2(g),并达到平衡。则: