题目内容
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,22.4LN2中含有的原子数为NA | |
| B. | 标准状况下,11.2 L CCl4中含有的分子数为0.5 NA | |
| C. | 物质的量浓度为1 mol•L-1的K2SO4溶液中,含2 NA个K+ | |
| D. | 23g Na与足量H2O反应转移的电子数为NA |
分析 A、求出氮气的物质的量,然后根据氮气为双原子分子;
B、标况下四氯化碳为液态;
C、溶液体积不明确;
D、求出钠的物质的量,然后根据反应后钠变为+1价来分析.
解答 解:A、标况下22.4L氮气的物质的量为1mol,而氮气为双原子分子,故1mol氮气中含2mol原子即2NA个,故A错误;
B、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、溶液体积不明确,故溶液中的钾离子的个数无法计算,故C错误;
D、23g钠的物质的量为1mol,而反应后钠变为+1价,故1mol钠失去1mol电子即NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
9.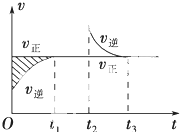 某恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
某恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
 某恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
某恒温密闭容器发生可逆反应:Z(?)+W(?)?X(g)+Y(?)△H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )| A. | Z和W在该条件下均为非气态 | |
| B. | t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等 | |
| C. | 若在该温度下此反应平衡常数表达式为K=c(X),则 t1~t2时间段与t3时刻后的X浓度不相等 | |
| D. | 若该反应只在某温度T以上自发进行,则该反应的平衡常数K随温度升高而减小 |
10.下列过程没有发生化学反应的是( )
| A. | 用煤液化和气化得到清洁燃料 | B. | 用热碱溶液清除炊具上残留的油污 | ||
| C. | 用氢氟酸来刻蚀玻璃器皿 | D. | 用活性炭去除冰箱中的异味 |
14.下列反应的离子方程式中,错误的是( )
| A. | 用稀硫酸清除铁锈:Fe2O3+6H+═2Fe3++3H2O | |
| B. | 铜粉放入硝酸银溶液里:Cu+2Ag+═Cu2++2Ag | |
| C. | 食盐水中滴加硝酸银溶液:Cl-+Ag+═AgCl↓ | |
| D. | 铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
4.有Al、CuO、Fe2O3组成的混合物共10.0g,放入500ml某浓度的盐酸溶液中,混合物全部溶解,当再加入250ml 2.00mol/L的NaOH溶液时,得到的沉淀最多.上述盐酸的物质的量浓度是( )
| A. | 0.500mol/L | B. | 1.00mol/L | C. | 2.00mol/L | D. | 3.00mol/L |
11.粗略测定草木灰中碳酸钾的含量,需经称量、溶解、过滤、蒸发等操作.下列图示对应的操作不规范的是( )
| A. |  称量 | B. |  溶解 | C. |  过滤 | D. |  蒸发 |