题目内容
纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
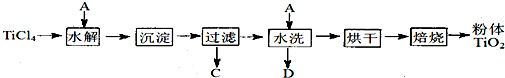
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·x H2O,经过滤、水洗除去其中的Cl,再烘干、焙烧除去水分得到粉体TiO2 。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+ ,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
⑴ TiCl4水解生成TiO2·x H2O的化学方程式为_______________________________。
⑵ 检验TiO2·x H2O中Cl-是否被除净的方法是______________________________。
⑶ 下列可用于测定TiO2粒子大小的方法是_____________________(填字母代号)。
a.核磁共振法 b.红外光谱法 c.质谱法 d.透射电子显微镜法
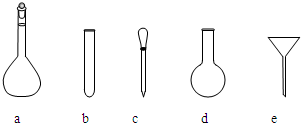
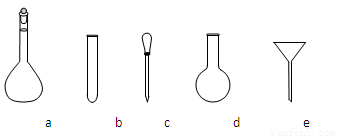
⑷ 配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是_________________;使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的_____(填字母代号)。
![]()
![]()
![]()
![]()
![]()
a b c d e
⑸ 滴定终点的现象是___________________________________________________。
⑹ 滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为_________________________。
⑺ 判断下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
① 若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果_________________________。
② 若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果_________。
(共18分)
⑴ TiCl4 + (x+2)H2O ![]() TiO2·xH2O↓ + 4HCl
TiO2·xH2O↓ + 4HCl
⑵ 取少量水洗液,滴加AgNO3溶液,不产生白色沉淀,说明Cl-已除净。
⑶ d
⑷ 抑制NH4Fe(SO4)2水解
a c
⑸ 溶液变为红色
⑹ ![]() (或
(或![]() %)
%)
⑺ ① 偏高 ② 偏低[来源:
解析:
本题考查盐类水解、实验分析技术、实验基本操作及实验数据的处理能力。
(1)根据盐类水解规律可知,Ti4+结合水电离的OH-形成TiO2的水合物,从元素守恒的角度不难写出相应的反应方程式。
(2)水解后的溶液为HCl溶液,故TiO2·xH2O表面吸附了Cl-,可通过检验洗涤液中是否存在Cl-确定沉淀是否洗涤干净。
(4)NH4Fe(SO4)2的阳离子均水解溶液呈酸性,故可以通过加H2SO4抑制它们的水解,防止所配溶液出现浑浊。容量瓶用于配置一定体积的溶液,滴管可以用来定容。
(5)当达到滴定终点,Fe3+与SCN-反应使溶液变为红色。
(6)根据元素守恒和电子守恒可知,有如下转化关系式:
TiO2~Ti3+~NH4Fe(SO4)2
M 1mol
m cv/1000
m=Mcv/1000,故TiO2的质量分数为:![]() 。
。
(7)从计算式可知,①所配浓度实际偏小,消耗溶液的体积偏大,测量值偏高。②俯视滴定管读数偏小,测量值偏小。


 TiO2?xH2O↓+4HCl
TiO2?xH2O↓+4HCl