题目内容
11.下列离子方程式正确的是( )| A. | 向水中通入氯气:Cl2+H2O═H++Cl-+HClO | |
| B. | 向明矾溶液中加过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 硫酸氢钠溶液中逐滴加入氢氧化钡溶液,至溶液恰好呈中性:Ba2++OH一+SO42-+H+═BaSO4↓+H2O | |
| D. | 溴乙烷与6mol/L氢氧化钠水溶液共热:C2H5Br+OH-CH2═CH2↑+Br-+H2O |
分析 A.次氯酸为弱电解质,应保留化学式;
B.不符合反应的客观事实,铝离子与氨水反应生成氢氧化铝和氨根离子;
C.硫酸氢钠溶液中逐滴加入氢氧化钡溶液,至溶液恰好呈中性,二者按2:1反应;
D.溴乙烷与6mol/L氢氧化钠水溶液共热发生取代反应,生成乙醇.
解答 解:A.向水中通入氯气,离子方程式:Cl2+H2O═H++Cl-+HClO,故A正确;
B.向明矾溶液中滴加过量氨水,氢氧化铝不溶于氨水,反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.硫酸氢钠溶液中逐滴加入氢氧化钡溶液,至溶液恰好呈中性,二者按2:1反应,离子方程式为Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O,故C错误;
D.溴乙烷与6mol/L氢氧化钠水溶液共热反应生成乙醇和溴化钠,离子方程式:C2H5Br+OH-→CH3-CH2-OH+Br-,故D错误;
故选:A.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意卤代烃发生取代反应和消去反应的条件为易错点,注意反应物用量对反应的影响,题目难度不大.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
1.化学与科学、技术、社会、环境密切相关.下列说法正确的是( )
| A. | 小苏打可以用作胃溃疡患者的胃酸中和剂 | |
| B. | 二氧化硫可以用来漂白纸浆、毛、丝、草帽辫、银耳、米粉等 | |
| C. | 飞机播撒碘化银或干冰可实现人工降雨 | |
| D. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅酸 |
2.将CuCl2、NaCl、AlCl3、FeCl2、FeCl3、NH4Cl、AgNO3七种溶液区分开,只用一种试剂,该试剂是( )
| A. | KSCN | B. | BaCl2 | C. | NaOH | D. | HCl |
19.某条件下,恒容密闭容器中发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);(正反应为放热反应),下列说法正确的是( )
| A. | 用高效催化剂,可提高CO2的利用率 | |
| B. | 单位时间内消耗CO2和H2的物质的量比为1:3时,反应达到平衡 | |
| C. | 及时分离出CH3OH和H2O可提高CO2和H2的利用率 | |
| D. | 升高温度可使该反应向正反应方向移动 |
6.乙醇在铜做催化剂条件下发生催化氧化时在何处断键( )


| A. | ① | B. | ② | C. | ③ | D. | ④ |
16.下列物质属于苯的同系物是( )
| A. | 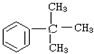 | B. |  | C. | 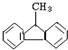 | D. | 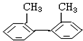 |
3.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的化学方程式:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性.反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色,该现象不能(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是过量的Cl2也可以将I-氧化为I2.
(5)装置F的作用是吸收多余的氯气,防止污染大气,其烧杯中的溶液 不能选用下列中的b(填字母编号).
a.饱和NaOH溶液
b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液
d.饱和Na2CO3溶液.

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的化学方程式:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)装置F的作用是吸收多余的氯气,防止污染大气,其烧杯中的溶液 不能选用下列中的b(填字母编号).
a.饱和NaOH溶液
b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液
d.饱和Na2CO3溶液.
20.下列描述中正确的是( )
| A. | 氮原子的价电子排布图: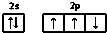 | |
| B. | 2p和3p轨道形状均为哑铃形,能量也相等 | |
| C. | 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素 | |
| D. | 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 |
1.元素周期表的一部分,针对表中的①…⑩中元素,填写下列空格:
(1)在这10种元素中,非金属性最强的元素是F,(填元素符号);
(2)比较①与②两种元素原子半径的大小,其中较大的是C(填元素符号);
(3)元素③与⑦的氢化物分别为HF和H2S(填化学式),两种氢化物的热稳定性大小为:前者>后者;(填“>”、“<”或“=”)
(4)元素④与⑤的最高价氧化物的水化物分别为Mg(OH)2和Al(OH)3(填化学式),两者的碱性大小为:前者>后者;(填“>”、“<”或“=”)
(5)写出工业上以元素⑦的单质为原料制取硫酸的化学方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3,SO3+H2O═H2SO4;
(6)元素①的原子结构示意图为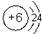 ,元素⑩的单质与氢气反应的化学方程式为N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
,元素⑩的单质与氢气反应的化学方程式为N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ⑩ | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)比较①与②两种元素原子半径的大小,其中较大的是C(填元素符号);
(3)元素③与⑦的氢化物分别为HF和H2S(填化学式),两种氢化物的热稳定性大小为:前者>后者;(填“>”、“<”或“=”)
(4)元素④与⑤的最高价氧化物的水化物分别为Mg(OH)2和Al(OH)3(填化学式),两者的碱性大小为:前者>后者;(填“>”、“<”或“=”)
(5)写出工业上以元素⑦的单质为原料制取硫酸的化学方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3,SO3+H2O═H2SO4;
(6)元素①的原子结构示意图为
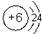 ,元素⑩的单质与氢气反应的化学方程式为N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
,元素⑩的单质与氢气反应的化学方程式为N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.