题目内容
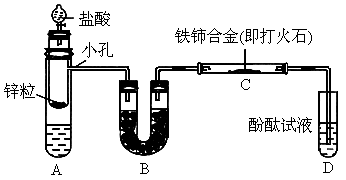
按图所示装置连接好仪器.
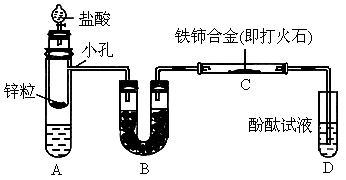
已知:A中装有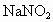 和
和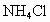 混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
C中发生反应的热化学方程式为: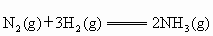 ;
;
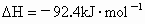
实验步骤如下:①检查装置的气密性;②用酒精灯加热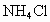 和
和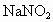 饱和溶液,待有气体生成,可停止加热,但仍有大量气体产生;③再用酒精灯给铁铈合金加热至一定温度;④从分液漏斗中滴入一定浓度盐酸,不久见酚酞试液变红.
饱和溶液,待有气体生成,可停止加热,但仍有大量气体产生;③再用酒精灯给铁铈合金加热至一定温度;④从分液漏斗中滴入一定浓度盐酸,不久见酚酞试液变红.
回答下列问题:
(1)写出A中两溶液间发生反应的化学方程式________,此反应为________热反应(填“放”或“吸”);
(2)先用酒精灯加热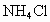 、
、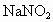 饱和溶液的目的是______________;
饱和溶液的目的是______________;
(3)C中铁铈合金的作用是______________,要先加热至一定温度的原因是______________;
(4)如果通入C中的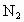 、
、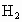 各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
答案:略
解析:
提示:
解析:
|
(1) (2) 产生 先排尽装置内的空气 先排尽装置内的空气
(3) 作催化剂, 、 、 要在一定温度才会开始反应,且催化剂在一定温度下催化效果最好 要在一定温度才会开始反应,且催化剂在一定温度下催化效果最好
(4)  不能完全反应掉,而且该反应是可逆反应,1 mol 不能完全反应掉,而且该反应是可逆反应,1 mol  与3mol 与3mol 不能生成2 mol 不能生成2 mol  ,故反应后放出的热量小于92.4 kJ. ,故反应后放出的热量小于92.4 kJ. |
提示:
|
通过 C中的反应物知A中反应产生 (另一试管发生Zn与盐酸反应产生 (另一试管发生Zn与盐酸反应产生 )从而可以写出A中反应方程式.从步骤②的题意中可知,该反应为放热反应.由于整个反应中要产生 )从而可以写出A中反应方程式.从步骤②的题意中可知,该反应为放热反应.由于整个反应中要产生 ,如有空气混入加热可能爆炸,所以先产生 ,如有空气混入加热可能爆炸,所以先产生 以排除空气,而后产生 以排除空气,而后产生 ,联系中学已学过的 ,联系中学已学过的 、 、 反应需催化剂,且为可逆反应,所以,(3)、(4)小题不难答出. 反应需催化剂,且为可逆反应,所以,(3)、(4)小题不难答出. |

练习册系列答案
相关题目




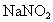 和
和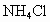 混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.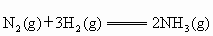 ;
;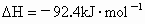
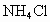 和
和 、
、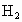 各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
 )如下:
)如下:
 (水杨酸)+SOCl2→
(水杨酸)+SOCl2→ (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑
 ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。