题目内容
已知T、X、Y、Z是中学化学常见的四种元素,其结构或性质信息如下表.

请根据信息回答有关问题:
(1)写出与Y2互为等电子体的分子式________.
(2)在相同状况下,Y的简单氢化物的沸点高于Z的氢化物,其原因是________.
(3)T、X、Y三种元素的电负性由大到小的顺序(填元素符号)是________.
(4)元素Q的原子序数是X与Z的原子序数之和.
①该元素基态原子的最外层电子排布式为________.
②元素Q与元素T、Y、Z分别形成平面型的[Q(TY)4]2-和四面体的[QZ4]2-,其中T与Y、Q与Z成键时中心原子采用的杂化方式分别是________.
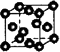
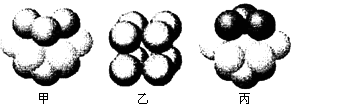
③元素Q形成的单质的晶体结构如下图所示,该晶体形成时的原子堆积方式是________(选填“甲”、“乙”、“丙”).
答案:
解析:
解析:
|
(1)CO(2分) (2)NH3分子间能形成氢键,而HCl分子间没有氢键(2分) (3)N>C>Na(2分) (4)①3d84s2(2分) ②sp、sp3(2分) ③丙(2分) |

练习册系列答案
相关题目


 数之和还多1。
数之和还多1。 。
。
