题目内容
5.下列变化中,需要加入还原剂才能实现的是( )| A. | Cl-→Cl2 | B. | H2→H+ | C. | CuO→Cu | D. | Zn→Zn2+ |
分析 变化中需要加入还原剂才能实现,说明给予物质作氧化剂,在反应中得电子化合价降低,据此分析解答.
解答 解:A.该反应中Cl元素化合价由-1价变为0价,所以氯离子是还原剂,需要氧化剂才能实现,如高锰酸钾、二氧化锰等,故A错误;
B.该反应中H元素化合价由0价变为+1价,所以氢气是还原剂,需要氧化剂才能实现,如氧气等,故B错误;
C.该反应中Cu元素化合价由+2价变为0价,所以CuO是氧化剂,需要还原剂才能实现,如C、CO等,故C正确;
D.该反应中Zn元素化合价由0价变为+2价,所以锌是还原剂,需要氧化剂才能实现,如硫酸等,故D错误;
故选C.
点评 本题考查氧化还原反应,侧重考查基本概念,明确氧化剂、还原剂概念内涵及其与化合价变化关系是解本题关键,熟悉常见元素化合价,题目难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
15.用两支惰性电极插入500mLAgNO3溶液中,通电电解.当电解液的pH从6.0变为3.0时(设电解时阴极没有氢气析出,且电解液在电解前后体积变化可以忽略),电极上析出银的质量大约是( )
| A. | 27mg | B. | 54mg | C. | 108mg | D. | 216mg |
16.根据物质的组成对物质进行分类,NaHCO3属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
13. 已知:Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
已知:Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
 已知:Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
已知:Na2O2(s)+CO2(g)═Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
| A. | CO的燃烧热为283 kJ | |
| B. | 2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g)△H=+452 kJ/mol | |
| C. | 如图可表示由CO生成CO2的反应过程和能量关系 | |
| D. | CO(g)与Na2O2(s)反应生成1molNa2CO3(s)时放出509kJ的热量 |
10.下列离子方程式正确的是( )
| A. | 向氨水中滴入盐酸:H++OH-=H2O | |
| B. | 向澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O | |
| C. | 稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 钠跟水反应:Na+2H2O=Na++2OH-+H2↑ |
17.下列物质中,物质的量为0.2mol的是( )
| A. | 16g氧气 | B. | 2g氢气 | ||
| C. | 4.48L氮气(标准状况) | D. | 6.02×1023个氯气分子 |
15.某溶液中可能含有下列5种离子中的某几种:Na+、NH4+、Mg2+、Al3+、Clˉ.为确认该溶液组成进行如下实验:①取20.0mL该溶液,加入25.0mL 4.00mol•L-1NaOH溶液,有白色沉淀、无剌激气味气体生成.过滤、洗涤、干燥,得沉淀1.16g.再将滤液稀释至100mL,测得滤液中c(OHˉ)为0.20mol•L-1;②另取20.0mL该溶液,加入足量的AgNO3溶液,生成白色沉淀11.48g.由此可得出关于原溶液组成的正确结论是( )
| A. | 一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+ | |
| B. | 一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+ | |
| C. | c(Clˉ)为 4.00mol•L-1,c(Al3+)为1.00 mol•L-1 | |
| D. | c(Mg2+)为 1.00mol•L-1,c(Na+)为 0.50 mol•L-1 |
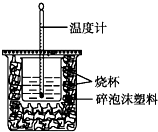 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.用50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: