题目内容
2.下列说法正确的是( )| A. | 固体硫酸钠不能导电,所以硫酸钠是非电解质 | |
| B. | 在NaOH溶液中除了Na+、OH-外,不存在其它粒子 | |
| C. | NaOH溶液能导电,所以NaOH溶液是电解质 | |
| D. | CO2、SO2、SO3、NH3等均属于非电解质 |
分析 A、电解质是在水溶液中或熔融状态下能导电的化合物;
B、氢氧化钠溶液是氢氧化钠溶于水得到的;
C、电解质是在水溶液中或熔融状态下能导电的化合物;
D、在水溶液中和熔融状态下均不导电的化合物为非电解质.
解答 解:A、电解质是在水溶液中或熔融状态下能导电的化合物,硫酸钠溶于水后和在熔融状态下均能导电,故为电解质,故A错误;
B、氢氧化钠溶液是氢氧化钠溶于水得到的,故氢氧化钠溶液中,除了钠离子和氢氧根离子,还有氢离子和水分子,故B错误;
C、电解质是在水溶液中或熔融状态下能导电的化合物,而氢氧化钠溶液为混合物,故不是电解质也不是非电解质,故C错误;
D、在水溶液中和熔融状态下均不导电的化合物为非电解质,CO2、SO2、SO3、NH3在熔融状态下均不导电,在溶液中导电和其本身无关,故为非电解质,故D正确.
故选D.
点评 本题考查了电解质、非电解质的概念和判断,难度不大,根据定义来分析即可.

练习册系列答案
相关题目
17. 甲~庚元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
 甲~庚元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚元素在周期表中的相对位置如图,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | 丙与戊的原子序数相差27 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 丁的最高价氧化物可用于制造光导纤维 | |
| D. | 常温下,甲和乙的单质均能与水剧烈反应 |
7.下列离子方程式正确的是( )
| A. | 碳酸钙和盐酸反应 CO32-+2H+═H2O+CO2↑ | |
| B. | 向氢氧化钡溶液中加入硫酸溶液 SO42-+Ba2+═BaSO4↓ | |
| C. | 向稀盐酸溶液中加铁 3Fe+6H+═3H2↑+3Fe3+ | |
| D. | 向硝酸银溶液中加盐酸 Ag++Cl-═AgCl↓ |
14.常温下,下列各组离子在特定溶液中一定能大量共存的是( )
| A. | 由水电离出的c(H+)=10-12 mol•L-1的溶液中:Na+、Cl-、HCO3-、SO42- | |
| B. | pH=12的澄清的溶液中:K+、Na+、MnO4-、SO42- | |
| C. | 甲基橙呈红色的溶液中:NH4+、Ba2+、AlO2-、Cl- | |
| D. | 加入少量铝粉后能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- |
11.下列各组中的离子,能在溶液中大量共存的是( )
| A. | Na+、K+、CO32-、NO3- | B. | Ca2+、CO32-、Na+、NO3- | ||
| C. | Na+、H+、NO3-、CO32- | D. | K+、Fe3+、OH-、NO3- |

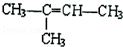 的名称是2-甲基-2-丁烯
的名称是2-甲基-2-丁烯 .
. .
.