题目内容
下列有关说法正确的是( )
| A、一定条件下,使用催化剂能加快反应速率但不能改变平衡转化率 | ||
| B、氢氧燃料电池的能量转换形式仅为化学能转化为电能 | ||
| C、在NH4HSO4溶液中由于NH4+的水解促进了水的电离,所以水的电离程度增大 | ||
D、在一密闭容器中发生2SO2+O2?2SO3反应,增大压强,平衡会正向移动,
|
考点:化学平衡的影响因素,反应热和焓变,盐类水解的应用
专题:基本概念与基本理论
分析:A、催化剂改变反应速率不改变化学平衡;
B、燃料电池中能量转化形式主要是化学能转化为电能,同时伴随热能等;
C、铵根离子水解促进水的电离,氢离子抑制水的电离程度大;
D、
的值为平衡常数计算,平衡常数随温度变化;
B、燃料电池中能量转化形式主要是化学能转化为电能,同时伴随热能等;
C、铵根离子水解促进水的电离,氢离子抑制水的电离程度大;
D、
| c2(SO3) |
| c2(SO2)?c(O2) |
解答:
解:A、催化剂改变反应速率不改变化学平衡,不能改变平衡转化率,故A正确;
B、燃料电池中能量转化形式主要是化学能转化为电能,同时伴随热能等,故B错误;
C、铵根离子水解促进水的电离,氢离子抑制水的电离程度大,所以水的电离程度减小,故C错误;
D、
的值为平衡常数计算,平衡常数随温度变化,增大压强不影响平衡常数,故D错误;
故选A.
B、燃料电池中能量转化形式主要是化学能转化为电能,同时伴随热能等,故B错误;
C、铵根离子水解促进水的电离,氢离子抑制水的电离程度大,所以水的电离程度减小,故C错误;
D、
| c2(SO3) |
| c2(SO2)?c(O2) |
故选A.
点评:本题考查了化学平衡、化学反应速率影响因素,原电池能量变化,盐类水解对水电离的影响,掌握基础是关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
化学与社会、环境、生活密切相关.下列说法正确的是( )
| A、食盐、食醋和味精是常用的食品添加剂,其主学成分均属钠盐 |
| B、SO2、C02、NO2均被列入我国空气质量报告的指标 |
| C、青铜是我国使用最早的合金 |
| D、家用84消毒液可用来漂白衣物,为了增强其漂白效果,使用时可加浓盐酸 |
“细节决定成败”对于下列实验细节处理正确的是( )
| A、实验室制氢气:为了加快反应速率,向稀H2SO4滴加少量CuSO4溶液 |
| B、钠与水的反应:取绿豆大小的金属钠放入烧杯,再滴入两滴酚酞试液,最后加入水 |
| C、配置0.10mol/L NaOH溶液:称取0.4g NaOH放入100mL容量瓶,加水至100mL |
| D、配置FeCl2溶液:称取一定量的FeCl2固体,加水溶解,在加入稀盐酸酸化 |
下列说法不正确的是( )
A、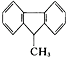 分子中的所有碳原子不可能同时在一个平面内 分子中的所有碳原子不可能同时在一个平面内 |
B、按系统命名法,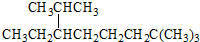 的名称为2,2,7-三甲基-6-乙基辛烷 的名称为2,2,7-三甲基-6-乙基辛烷 |
C、目前市场上大量矿泉水、食用油等产品包装瓶几乎都是用PET(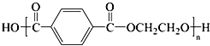 )的合成单体之一是对苯二甲酸 )的合成单体之一是对苯二甲酸 |
| D、有一种信息素的结构简式为CH3(CH2)5CH═CH(CH2)9CHO,为验证该物质中既含有醛基又含有碳碳双键,向该物质的试液中先加过量的溴水溶液,观察到溶液褪色,再向溶液中加入新制的Cu(OH)2悬浊液,加热煮沸,观察到砖红色沉淀 |
白藜芦醇 广泛存在于食物(例如桑葚、花生,尤其是葡萄中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )
广泛存在于食物(例如桑葚、花生,尤其是葡萄中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )
 广泛存在于食物(例如桑葚、花生,尤其是葡萄中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )
广泛存在于食物(例如桑葚、花生,尤其是葡萄中,它可能具有抗癌性.能够跟1mol该化合物起反应的Br2或H2的最大用量分别是( )| A、1mol,1mol |
| B、3.5mol,7mol |
| C、3.5mol,6mol |
| D、6mol,7mol |
 短周期元素R、T、Q、W、Z在元素周期表中的相对位置如下图所示,五种元素中只有一种金属元素.下列判断错误的是( )
短周期元素R、T、Q、W、Z在元素周期表中的相对位置如下图所示,五种元素中只有一种金属元素.下列判断错误的是( )| A、W的单质易溶于CS2 |
| B、Q与R可能形成化合物Q3R4 |
| C、T的最高价氧化物的对应水化物为强碱 |
| D、W、Z都有多种含氧酸 |
下列反应中离子方程式的书写正确的是( )
| A、向Na2CO3溶液中逐滴滴加盐酸:2H++CO32-═CO2↑+H2O |
| B、向FeCl3溶液中通入H2S气体:Fe3++H2S═Fe2++S↓+2H+ |
| C、向碳酸氢钠溶液中滴加过量的澄清石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、浓度均为0.1mol/L的硫酸氢铵与氢氧化钠两种溶液等体积混合:NH4++HSO4-+2OH-═SO42-+NH3↑+2H2O |
某同学将一小块金属钠投入到硫酸铜溶液中,通过此实验不能证明下列性质中的( )
| A、钠比水轻但比煤油重 |
| B、钠的熔点较低 |
| C、钠与水反应时要放出热量 |
| D、钠与水反应后溶液呈碱性 |
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、7.8g Na2O2所含的阴离子数目为2NA |
| B、在熔融状态下,lmol KHSO4完全电离出的阳离子数目为2NA |
| C、14g乙烯和丙烯的混和气体中共含有3NA对共用电子对 |
| D、将分子总数为NA的NH3和HCl的混合气体置于标准状况下,其体积为约22.4L |