题目内容
3.下列关于氧化还原反应的叙述,正确的是( )| A. | 失去电子的反应是还原反应 | |
| B. | 在氧化还原反应中不一定所有的元素的化合价都发生变化 | |
| C. | 做氧化剂的物质不能是还原剂 | |
| D. | 发生还原反应的元素对应产物是氧化产物 |
分析 A.失电子发生氧化反应;
B.氧化还原反应中一定存在元素的化合价变化,可能为同种元素,也可能为不同元素;
C.氧化还原反应中氧化剂和还原剂可能是同种物质;
D.发生还原反应生成的产物为还原产物.
解答 解:A.失电子元素的化合价升高发生氧化反应,得电子元素的化合价降低发生还原反应,故A错误;
B.反应2H2S+SO2═3S↓+2H2O中,H、O元素的化合价不变,只有S元素发生变价,则反应中不一定所有元素的化合价都发生变化,故B正确;
C.氧化还原反应中氧化剂和还原剂可能是同种物质,如氯酸钾分解生成氯化钾和氧气,氯酸钾即是氧化剂又是还原剂,故C错误;
D.发生还原反应生成的产物为还原产物,发生氧化反应的元素对应产物是氧化产物,故D错误.
故选B.
点评 本题考查氧化还原反应及常见的化学反应,题目难度不大,侧重于基础知识的考查,根据化合价的变化分析,注意举例分析.

练习册系列答案
相关题目
13.将一小块金属钠投入足量的下列溶液中,既能生成气体,又能生成白色沉淀的是( )
| A. | 稀盐酸 | B. | Ba(OH)2稀溶液 | C. | MgCl2溶液 | D. | CuSO4溶液 |
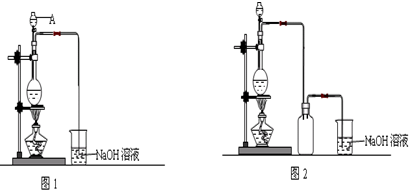
14. 下列气体在足量的氧气中充分燃烧,产生二氧化碳和水两种物质,将产物依次通过如图中A、B装置,经完全吸收后,测得浓硫酸质量增加9g,氢氧化钠溶液增加11g,则气体可能是下列气体中的( )
下列气体在足量的氧气中充分燃烧,产生二氧化碳和水两种物质,将产物依次通过如图中A、B装置,经完全吸收后,测得浓硫酸质量增加9g,氢氧化钠溶液增加11g,则气体可能是下列气体中的( )
 下列气体在足量的氧气中充分燃烧,产生二氧化碳和水两种物质,将产物依次通过如图中A、B装置,经完全吸收后,测得浓硫酸质量增加9g,氢氧化钠溶液增加11g,则气体可能是下列气体中的( )
下列气体在足量的氧气中充分燃烧,产生二氧化碳和水两种物质,将产物依次通过如图中A、B装置,经完全吸收后,测得浓硫酸质量增加9g,氢氧化钠溶液增加11g,则气体可能是下列气体中的( )| A. | C2H2 | B. | C2H5OH 蒸汽 | ||
| C. | CH4 | D. | CH4与H2的混合气体 |
11.下列叙述正确的是( )
| A. | 6.02×1023个碳-12原子就是阿伏加德罗常数 | |
| B. | 1mol氧含6.02×1023个O2分子 | |
| C. | 1molCaCl2中含3mol离子 | |
| D. | 0.5molCl2含1mol氯 |
15.下列转变需加入还原剂的是( )
| A. | CO→CO2 | B. | FeCl2 →FeCl3 | C. | Na2SO3 →SO2 | D. | CuO→Cu |