题目内容
4.下列解释事实的化学方程式或离子方程式,不正确的是( )| A. | 工业上可用电解法制备Mg:MgCl2$\frac{\underline{\;熔融\;}}{电解}$ Mg+Cl2↑ | |
| B. | 用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+Fe2++14H+═2Cr3++Fe3++7H2O | |
| C. | 等浓度的NH4Al(SO4)2溶液与Ba(OH)2溶液以1:2体积比混合出现白色沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+NH3•H2O+Al(OH)3↓ | |
| D. | 自然界中正常的雨水呈酸性:H2O+CO2?H2CO3?H++HCO3- |
分析 A.Mg为活泼金属,电解熔融氯化镁冶炼Mg;
B.电子、电荷不守恒;
C.以1:2体积比混合,反应生成硫酸钡、氢氧化铝和一水合氨;
D.雨水中溶解二氧化碳,生成碳酸电离显酸性.
解答 解:A.Mg为活泼金属,电解熔融氯化镁冶炼Mg,电解反应为MgCl2$\frac{\underline{\;熔融\;}}{电解}$ Mg+Cl2↑,故A正确;
B.用FeSO4除去酸性废水中的Cr2O72-的离子反应为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,故B错误;
C.等浓度的NH4Al(SO4)2溶液与Ba(OH)2溶液以1:2体积比混合出现白色沉淀,离子反应为NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+NH3•H2O+Al(OH)3↓,故C正确;
D.雨水中溶解二氧化碳,生成碳酸电离显酸性,反应为H2O+CO2?H2CO3?H++HCO3-,故D正确;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒分析,题目难度不大.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
14.2015年2月28日,央视原记者柴静及其团队制作的视频《穹顶之下》引起了人们对环境保护的再思考,下列说法体现人与自然和谐相处的是( )
| A. | 将聚氯乙烯等塑料垃圾焚烧 | |
| B. | 推广矿物燃料脱硫技术以减少SO2等有害气体的排放 | |
| C. | 大力开采石油、煤、页岩气(主要成分为CH4)等化石燃料 | |
| D. | 电池使用后随意丢弃,无需处理 |
15.下列变化,需要加入适当的氧化剂才能完成的是( )
| A. | PCl3→PCl5 | B. | MnO4-→Mn2+ | C. | SO2→SO32- | D. | FeCl3→FeCl2 |
3.下列化学用语中,书写或说法正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | |
| B. | 丙烷的球棍模型为 | |
| C. | 乙醇含有的官能团是-OH,带一个单位负电荷 | |
| D. | 乙酸的分子式为C2H4O2,其中CH3-在溶液中能电离出H+ |
20.取pH=2的盐酸和醋酸各100毫升,再分别加入0.65克锌粉,在相同条件下充分反应后,有关叙述正确的是( )
| A. | 刚开始醋酸与锌反应速率大 | |
| B. | 反应过程中盐酸和醋酸分别与锌反应的速率一样大 | |
| C. | 醋酸与锌反应放出的氢气多 | |
| D. | 锌分别与醋酸、盐酸反应产生的氢气一样多 |
1.下列说法正确的是( )
| A. | 红宝石、蓝宝石的主要成分是Al2O3,石英玻璃、分子筛的主要成分是硅酸盐 | |
| B. | 肌红蛋白、蚕丝、过氧化氢酶、鱼肝油充分水解后均可得到氨基酸 | |
| C. | 2014年1月,国家首次将雾霾天气纳入自然灾情进行通报,雾霾是一种分散系,其分散剂为空气 | |
| D. | 二氧化碳、氨气、盐酸、食盐在一定条件下均能导电,但只有盐酸和食盐属于电解质,二氧化碳和氨气属于非电解质 |
 将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见氧化物,气体E是单质F所含元素的氢化物.
将晶体X加热分解,可得A、B、D、E、F和水六种产物,其中A、B、D都是中学化学中常见氧化物,气体E是单质F所含元素的氢化物. ;
; (写结构简式),它的一氯代物有1种.
(写结构简式),它的一氯代物有1种.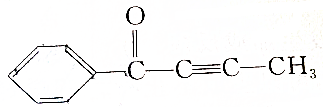 ,请回答下列问题:
,请回答下列问题: