题目内容
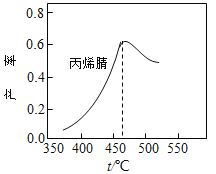
【题目】在容积固定的密闭容器中,以丙烯、氨、氧气为原料,在催化剂存在下生产丙烯腈(C3H3N),反应的热化学方程式为:2C3H6(g)+2NH3(g)+3O2(g) ![]() 2C3H3N(g)+6H2O(g) △H= -1030kJ·mol-1。在其他条件和反应时间相同时,丙烯腈产率与反应温度的关系曲线如图所示。下列有关说法错误的是( )
2C3H3N(g)+6H2O(g) △H= -1030kJ·mol-1。在其他条件和反应时间相同时,丙烯腈产率与反应温度的关系曲线如图所示。下列有关说法错误的是( )
A.低于460℃时,丙烯腈的产率随温度升高而升高,是因为升高温度,反应速率加快
B.高于460℃时,丙烯腈的产率随温度升高而降低,可能与温度度升高,化学平衡逆向移动有关
C.其他条件不变,降低温度有利于提高丙烯腈平衡产率
D.投料比不变,增加反应物的浓度有利于提高丙烯腈平衡产率
【答案】D
【解析】
反应时间相同情况下,温度越高,反应速率越快,越先达到平衡,460℃时产率最高,此时此温度下反应达平衡,低于460℃,速率太慢,没有达到平衡,高于460℃,温度升高,平衡移动。
A.低于460℃,速率慢,没有达到平衡,随着温度升高,反应速率加快,从而丙烯腈的产量提高,A不符合题目要求,A项错误;
B.460℃时反应达平衡,该反应是放热反应,温度升高平衡逆向移动,丙烯腈的产率降低,B不符合题目要求,,B项错误;
C.其他条件不变,降低温度,平衡正向移动,提高丙烯腈平衡产率, C不符合题目要求,C项错误;
D.该反应正向是气体分子数增多的方向,投料比不变,增加反应物的浓度相当于加压,加压平衡向气体分子数减少的方向即逆向移动,降低丙烯腈平衡产率,D符合题目要求,D项正确;
答案选D。

【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯, 易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 易升华 | |
沸点/℃ | 132 | 173 | ||
(1)用H2还原无水FeCl3制取FeCl2。有关装置如下:

①H2还原无水FeCl3制取FeCl2的化学方程式为_____________。
②按气流由左到右的方向,上述仪器的连接顺序为_________(填字母,装置可多次使用);C中盛放的试剂是_____________。
③该制备装置的缺点为________________。
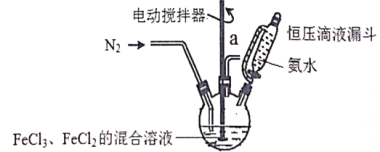
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按下图装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的名称是__________。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是____,回收滤液中C6H5C1的操作方法是______。
③反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol/LNaOH溶液滴定,终点时消耗NaOH溶液为19.60 mL,则氯化铁的转化率为__________。
④为了减少实验误差,在制取无水FeCl2过程中应采取的措施有:________(写出一点即可)。
【题目】以下是25℃时几种难溶电解质的溶解度:
难溶电解质 | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
溶解度/g | 9×10-4 | 1.7×10-6 | 1.5×10-4 | 3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子.如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,再加入一定量的试剂反应,过滤结晶即可;
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的氢氧化镁,充分反应,过滤结晶即可;
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶即可.
请回答下列问题:
(1)上述三个除杂方案都能够达到很好的效果,Fe2+、Fe3+都被转化为____________(填化学式)而除去.
(2)①中加入的试剂应该选择________为宜,其原因是__________.
(3)②中除去Fe3+所发生的总反应的离子方程式为______________________________.
(4)下列与方案③相关的叙述中,正确的是______(填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质,不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜或氧化铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+一定不能大量存在