��Ŀ����
��1����V mL NO ��NO2 �Ļ������ͨ��ˮ���պõ�a mL��ɫ����A��������ɫ����A��������O2 ��ϣ�ͨ��ˮ������պõ�5mL ��ɫ����B���Իش�
��A������______��B������______��
��A����������______mL��
��2�����ݾ����Ե�Ҫ�����ʵ�鷽������4mol����Alȫ��ת��ΪAl��OH��3����������HCl a mol��NaOH b mol����a+b���������ֵΪ______��
�⣺��1����NO��ˮ����Ӧ��3NO2+H2O=2HNO3+NO������NO ��NO2 �Ļ������ͨ��ˮ���պõ�����ɫ������NO��һ��������������ˮ��Ӧ����ʽΪ��4NO+3O2+2H2O=4HNO3���÷�Ӧ��NO��O2�����֮��Ϊ4��3����NO��������O2 ��ϣ�ͨ��ˮ������պ�������ʣ�࣬���Եõ�����ɫ����B��������
�ʴ�Ϊ��NO��O2��
��ͨ�����Ϸ���֪��ʣ���B����������������4NO+3O2+2H2O=4HNO3֪���������һ��������������ˮ��Ӧ��ʣ�������ռ����������� �������������������5mL��
�������������������5mL�� =20mol������A�������������ȣ�����Ҳ��20mL���ʴ�Ϊ��20��
=20mol������A�������������ȣ�����Ҳ��20mL���ʴ�Ϊ��20��
��2���������ᡢ�������Ʒ�Ӧ����ʽ�ֱ�Ϊ��2Al+6HCl=2AlCl3+3H2���١�2NaOH+2Al+2H2O=2NaAlO2+3H2���ڣ�
�Ȼ�����ƫ��������Һ�����ķ�ӦΪ��6H2O+AlCl3+3NaAlO2=4Al��OH��3��+3NaCl�ۣ�Ҫʹ4mol����Alȫ��ת��ΪAl��OH��3�������ɵ��Ȼ�����ƫ������ǡ�÷�Ӧ���������������ɣ�
������ʽ�١�2+�ڡ�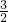 �ã�
�ã�
4Al+3HCl+3NaOH+3H2O=AlCl3+3NaAlO2+6H2����
������ʽ��+�ܵã�4Al+3HCl+3NaOH+9H2O=4Al��OH��3+3NaCl+6H2����
���ݷ���ʽ4Al+3HCl+3NaOH+9H2O=4Al��OH��3+3NaCl+6H2����������������Ƶļ�����֮����6�����ԣ�a+b���������ֵ��6���ʴ�Ϊ��6��
��������1��һ��������ˮ����Ӧ������������ˮ��Ӧ����һ�����������ᣬ�ݴ��ж�A����ɷ֣�����һ��������������ˮ��Ӧ����ʽȷ��B����ɷ֣����ò���������A����������
��2���������ᡢ�������Ʒ�Ӧ����ʽ�ֱ�Ϊ��2Al+6HCl=2AlCl3+3H2���١�2NaOH+2Al+2H2O=2NaAlO2+3H2���ڣ�
�Ȼ�����ƫ��������Һ�����ķ�ӦΪ��6H2O+AlCl3+3NaAlO2=4Al��OH��3��+3NaCl�ۣ�Ҫʹ4mol����Alȫ��ת��ΪAl��OH��3�������ɵ��Ȼ�����ƫ������ǡ�÷�Ӧ���������������ɣ�
������ʽ�١�2+�ڡ�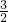 �ã�
�ã�
4Al+3HCl+3NaOH+3H2O=AlCl3+3NaAlO2+6H2����
������ʽ��+�ܵã�4Al+3HCl+3NaOH+9H2O=4Al��OH��3+3NaCl+6H2����
���ݷ���ʽ4Al+3HCl+3NaOH+9H2O=4Al��OH��3+3NaCl+6H2�� ȷ��������������Ƶ������ֵ��
���������⿼���˸��ݷ���ʽ�ļ��㣬�ѵ��Ǽ��㣨2���У�a+b���������ֵ����ȷ��Ҫʹ4mol����Alȫ��ת��ΪAl��OH��3�������ɵ��Ȼ�����ƫ������ǡ�÷�Ӧ���������������ǽⱾ��Ĺؼ���
�ʴ�Ϊ��NO��O2��
��ͨ�����Ϸ���֪��ʣ���B����������������4NO+3O2+2H2O=4HNO3֪���������һ��������������ˮ��Ӧ��ʣ�������ռ�����������
 �������������������5mL��
�������������������5mL�� =20mol������A�������������ȣ�����Ҳ��20mL���ʴ�Ϊ��20��
=20mol������A�������������ȣ�����Ҳ��20mL���ʴ�Ϊ��20����2���������ᡢ�������Ʒ�Ӧ����ʽ�ֱ�Ϊ��2Al+6HCl=2AlCl3+3H2���١�2NaOH+2Al+2H2O=2NaAlO2+3H2���ڣ�
�Ȼ�����ƫ��������Һ�����ķ�ӦΪ��6H2O+AlCl3+3NaAlO2=4Al��OH��3��+3NaCl�ۣ�Ҫʹ4mol����Alȫ��ת��ΪAl��OH��3�������ɵ��Ȼ�����ƫ������ǡ�÷�Ӧ���������������ɣ�
������ʽ�١�2+�ڡ�
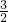 �ã�
�ã�4Al+3HCl+3NaOH+3H2O=AlCl3+3NaAlO2+6H2����
������ʽ��+�ܵã�4Al+3HCl+3NaOH+9H2O=4Al��OH��3+3NaCl+6H2����
���ݷ���ʽ4Al+3HCl+3NaOH+9H2O=4Al��OH��3+3NaCl+6H2����������������Ƶļ�����֮����6�����ԣ�a+b���������ֵ��6���ʴ�Ϊ��6��
��������1��һ��������ˮ����Ӧ������������ˮ��Ӧ����һ�����������ᣬ�ݴ��ж�A����ɷ֣�����һ��������������ˮ��Ӧ����ʽȷ��B����ɷ֣����ò���������A����������
��2���������ᡢ�������Ʒ�Ӧ����ʽ�ֱ�Ϊ��2Al+6HCl=2AlCl3+3H2���١�2NaOH+2Al+2H2O=2NaAlO2+3H2���ڣ�
�Ȼ�����ƫ��������Һ�����ķ�ӦΪ��6H2O+AlCl3+3NaAlO2=4Al��OH��3��+3NaCl�ۣ�Ҫʹ4mol����Alȫ��ת��ΪAl��OH��3�������ɵ��Ȼ�����ƫ������ǡ�÷�Ӧ���������������ɣ�
������ʽ�١�2+�ڡ�
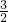 �ã�
�ã�4Al+3HCl+3NaOH+3H2O=AlCl3+3NaAlO2+6H2����
������ʽ��+�ܵã�4Al+3HCl+3NaOH+9H2O=4Al��OH��3+3NaCl+6H2����
���ݷ���ʽ4Al+3HCl+3NaOH+9H2O=4Al��OH��3+3NaCl+6H2�� ȷ��������������Ƶ������ֵ��
���������⿼���˸��ݷ���ʽ�ļ��㣬�ѵ��Ǽ��㣨2���У�a+b���������ֵ����ȷ��Ҫʹ4mol����Alȫ��ת��ΪAl��OH��3�������ɵ��Ȼ�����ƫ������ǡ�÷�Ӧ���������������ǽⱾ��Ĺؼ���

��ϰ��ϵ�д�
�����Ŀ

 þ�����Ļ�����м���������ϡ���ᣬǡ����ȫ��Ӧ���ɱ�״���µ�����bL����Ӧ�����Һ�м���c mol��L-1����������ҺV mL��ʹ�������Ӹպó�����ȫ���õ��ij�������Ϊn g���ٽ��õ��ij����������������ٸı�Ϊֹ���õ�����p g�������й�ϵ����ȷ����
þ�����Ļ�����м���������ϡ���ᣬǡ����ȫ��Ӧ���ɱ�״���µ�����bL����Ӧ�����Һ�м���c mol��L-1����������ҺV mL��ʹ�������Ӹպó�����ȫ���õ��ij�������Ϊn g���ٽ��õ��ij����������������ٸı�Ϊֹ���õ�����p g�������й�ϵ����ȷ���� B��
B�� C��
C�� D��
D��