题目内容
下列溶液稀释至100ml后溶液中c(Cl-)最大的是
- A.30mL 0.5mol/L AlCl3溶液
- B.10mL 2.5mol/L KCl溶液
- C.10mL 3mol/L NaCl溶液
- D.20mL 1mol/L MgCl2溶液
A
分析:根据稀释定律,稀释前后氯离子物质的量不变,计算稀释后氯离子浓度,据此结合选项解答.
电解质溶液离子浓度=电解质浓度×电解质电离出离子的数目,与溶液的体积无关,计算选项中氯离子的浓度,进行判断.
解答:A、30mL 0.5mol/L AlCl3溶液中c(Cl-)=0.5mol/L×3=1.5mol/L,稀释至100ml后溶液中c(Cl-)=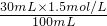 =0.45mol/L;
=0.45mol/L;
B、10mL 2.5mol/L KCl溶液中c(Cl-)=2.5mol/L×1=2.5mol/L,稀释至100ml后溶液中c(Cl-)=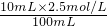 =0.25mol/L;
=0.25mol/L;
C、10mL 3mol/L NaCl溶液中c(Cl-)=3mol/L×1=3mol/L,稀释至100ml后溶液中c(Cl-)=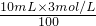 =0.3mol/L;
=0.3mol/L;
D、20mL 1mol/L MgCl2溶液中c(Cl-)=1mol/L×2=2mol/L,稀释至100ml后溶液中c(Cl-)=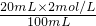 =0.4mol/L;
=0.4mol/L;
故选A.
点评:本题考查离子浓度的计算,难度不大,注意根据稀释定律计算稀释后氯离子浓度进行解答.
分析:根据稀释定律,稀释前后氯离子物质的量不变,计算稀释后氯离子浓度,据此结合选项解答.
电解质溶液离子浓度=电解质浓度×电解质电离出离子的数目,与溶液的体积无关,计算选项中氯离子的浓度,进行判断.
解答:A、30mL 0.5mol/L AlCl3溶液中c(Cl-)=0.5mol/L×3=1.5mol/L,稀释至100ml后溶液中c(Cl-)=
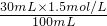 =0.45mol/L;
=0.45mol/L;B、10mL 2.5mol/L KCl溶液中c(Cl-)=2.5mol/L×1=2.5mol/L,稀释至100ml后溶液中c(Cl-)=
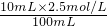 =0.25mol/L;
=0.25mol/L;C、10mL 3mol/L NaCl溶液中c(Cl-)=3mol/L×1=3mol/L,稀释至100ml后溶液中c(Cl-)=
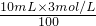 =0.3mol/L;
=0.3mol/L;D、20mL 1mol/L MgCl2溶液中c(Cl-)=1mol/L×2=2mol/L,稀释至100ml后溶液中c(Cl-)=
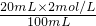 =0.4mol/L;
=0.4mol/L;故选A.
点评:本题考查离子浓度的计算,难度不大,注意根据稀释定律计算稀释后氯离子浓度进行解答.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目