题目内容
【题目】在一定温度下,1 mol CO和2 mol H2O通入一个密闭容器中:CO(g)+H2O (g)![]() CO2(g)+H2(g),一定时间后达到平衡,此时,CO的含量为p%,若维持温度不变,改变起始加入物质的物质的量,平衡时CO的含量仍为p%的是( )
CO2(g)+H2(g),一定时间后达到平衡,此时,CO的含量为p%,若维持温度不变,改变起始加入物质的物质的量,平衡时CO的含量仍为p%的是( )
A.1 mol CO2、2 mol H2B.0.2 mol CO2、0.2 mol H2、0.8 mol CO、1.8 mol H2O
C.1 mol CO2、1 mol H2OD.1 mol CO2、 1 mol H2、 2 mol H2O
【答案】B
【解析】
维持温度不变,改变起始加入物质的物质的量,平衡时CO的含量仍为p%,说明二者互为等效平衡,该反应为气体等体积反应,“一边倒”后,需满足n(CO):n(H2O)=1:2即可。
A、1 mol CO2、2 mol H2转化到左边,得到n(CO)=1mol、n(H2O)=1mol、n(H2)=1mol,与原平衡不等效,故A不符合;
B、0.2 mol CO2、0.2 mol H2、0.8 mol CO、1.8 mol H2O转化到左边,得到n(CO)=1mol、n(H2O)=2mol,与原平衡完全等效,故B符合;
C、CO2与H2O充入后不能发生CO(g)+H2O (g)![]() CO2(g)+H2(g),故C不符合;
CO2(g)+H2(g),故C不符合;
D、1 mol CO2、 1 mol H2、 2 mol H2O转化到左边,得到n(CO)=1mol、n(H2O)=3mol,与原平衡不等效,故D不符合;
答案选B。

【题目】硼是动植物所必须的微量元素,其单质和化合物广泛应用于冶金、机械、化工、核工业、医药、农业等部门。利用硼镁矿(主要成分为Mg2B2O3·5H2O)制取制硼酸、金属镁及粗硼的工艺流程图如下:
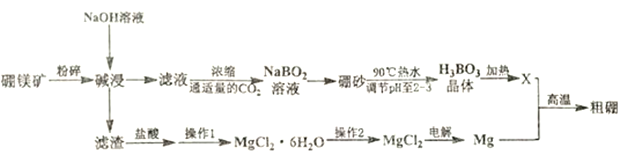
已知:①硼砂为Na2B4O7·10H2O
②硼酸(H3BO3)是一种可溶于水的一元弱酸,与过量的NaOH反应生成Na[B(OH)4]
③硼酸在不同温度下的溶解度:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度(g/100g水) | 3 | 3 | 5 | 7 | 9 | 11 | 15 | 18 | 23 | 29 |
(1)粉碎硼铁矿的目的是:______________;Mg2B2O5·H2O中B的化合价为:______价。
(2)滤渣的主要成分是: ________
(3)硼酸的电子式: ________;写出硼酸在水中电离的方程式: ________________;
(4)X为硼酸晶体加热完全脱水后的产物,其与Mg反应制取粗硼的化学方程式为: ________;
(5)硼砂溶于90℃热水后,常用稀硫酸调pH至2~3(酸性)制取HBO3晶体,该反应的离子方程式为: ________________;从上述溶液中获得H3BO3晶体的操作: ________________。