题目内容
1.化学与生产、生活密切相关.下列叙述正确的是( )| A. | 采用催化措施,将汽车尾气中的CO和NO转化为无害气体 | |
| B. | 合金材料中不可能含有非金属元素 | |
| C. | 信息产业中的光缆的主要成分是单质硅 | |
| D. | 14C可用于文物年代的鉴定,14C与12C互为同素异形体 |
分析 A.汽车尾气中的一氧化碳和一氧化氮在催化剂作用下反应生成无污染的气体二氧化碳和氮气;
B.依据合金概念就是两种或两种以上的金属(或金属跟非金属)熔合而成的具有金属特性的物质;
C.光缆的主要成分是二氧化硅;
D.同素异形体是同种元素组成的不同的单质.
解答 解:A.汽车尾气中的一氧化碳和一氧化氮在催化剂作用下反应生成无污染的气体二氧化碳和氮气,采用催化措施,将汽车尾气中的CO和NO转化为无害气体,故A正确;
B.合金材料中可能含有金属元素,非金属元素,如生铁含有碳,故B错误;
C.信息产业中的光缆的主要成分是二氧化硅,故C错误;
D.14C与12C互为同位素,同素异形体是单质,故D错误.
故选A.
点评 本题考查了合金、汽车尾气、光导纤维等物质的性质分析,积累化学知识,掌握同位素、同素异形体概念的区别是解题关键,题目难度中等.

练习册系列答案
相关题目
12.下列说法错误的是( )
| A. | 等物质的量的NaX和弱酸HX混合后的溶液中c(HX)可能大于c(X-) | |
| B. | 在pH=4.5的NaHSO3溶液中,c(H2SO3)大于c(SO32-) | |
| C. | 向0.1 mol/L醋酸溶液中加水稀释的过程中c(OH-)不断增大 | |
| D. | 向含有Na2SO4的BaSO4悬浊液中加水稀释,c(Ba2+)增大 |
9.下列实验操作对应的实验现象及解释或结论都正确的是( )
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 用某无色溶液进行焰色反应 | 焰色呈黄色 | 原溶液一定是钠盐溶液 |
| B | 向NaOH溶液中滴加足量的MgCl2 溶液,然后再滴加足量的CuCl2溶液 | 先产生白色沉淀, 然后沉淀变蓝色 | KSP[Cu(OH)2]>KSP[Mg(OH)2] |
| C | 将水蒸汽通过灼热的铁粉 | 粉末变红 | 铁与水蒸汽在高温下发生 反应 |
| D | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2(g)═N2O4(g) △H<0 |
| A. | A | B. | B | C. | C | D. | D |
6.常温下,某无色溶液用激光笔照射无丁达尔现象,加入FeCl3后溶液显色.下列各组微粒在此溶液可以大量共存的是( )
| A. | Na+、K+、Fe2+、Cl- | B. | K+、Fe3+、NO3-、Fe(OH)3(胶体) | ||
| C. | Cl-、SCN-、NH4+、葡萄糖分子 | D. | OH-、Na+、苯酚、Br - |
13.设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,11.2 L SO3所含的氧原子数为1.5NA | |
| B. | 电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA | |
| C. | 常温常压下,7.8 gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8 NA | |
| D. | 在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
15.下列说法不正确的是( )
| A. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、普通玻璃棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2-3 次的实验平均值等措施,以达到良好的实验效果 | |
| B. | 容量瓶、量筒和滴定管上都标有使用温度;量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| C. | pH计能用于酸碱中和滴定终点的判断 | |
| D. | 在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 |
 二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向.
二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向.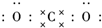 ,所含化学键的类型是共价键.
,所含化学键的类型是共价键.


