题目内容
10.一定温度下,100mL 6mol/L H2SO4与过量锌粉反应,由于反应太快,不易操作.为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )| A. | K2SO4固体 | B. | H2O | C. | 少量CuSO4溶液 | D. | 4 mol/L H2SO4 |
分析 过量的锌粉反应,硫酸完全反应,为了减缓反应速率但又不影响生成氢气的总量,可减小氢离子浓度但不改变其物质的量,以此来解答.
解答 解:A.加硫酸钾固体,不反应,不会改变氢离子浓度,反应速率不变,生成氢气的量不变,故A不选;
B.加水,减小氢离子浓度但不改变其物质的量,反应速率减小,生成氢气的量不变,故B选;
C.锌置换出铜,形成原电池反应,反应速率增大,故C不选;
D.加入4 mol/L H2SO4与过量锌粉反应,生成氢气的总量会增加,故D不选.
故选B.
点评 本题考查影响化学反应速率的因素,为高频考点,注意信息中Zn过量及浓度对反应速率的影响即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
1.下列表示物质结构的化学用语正确的是( )
| A. | 8个中子的碳原子的核素符号:12C | B. | 氮气的电子式: | ||
| C. | Cl-离子的结构示意图: | D. | NaCl的电子式: |
18.下列化学用语中,不正确的是( )
| A. | CO2的电子式: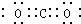 | B. | 乙炔分子的结构式H-C≡C-H | ||
| C. | H2O分子的比例模型  | D. | Clˉ离子的结构示意图: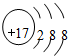 |
5.分类法是一种行之有效、简单易行的科学方法.某同学用下表所示形式对所学知识进行分类,其中甲与乙关系正确的是( )
| 选项 | 甲 | 乙 |
| A | 电解质 | BaSO4、NaHSO4、SO3 |
| B | 弱电解质的电离 | 均分步电离 |
| C | 化学平衡影响因素 | 温度、压强、浓度、催化剂等 |
| D | 化学电源 | 一次电池、二次电池、燃料电池等 |
| A. | A | B. | B | C. | C | D. | D |
19.某稀溶液中含有HCO3-、SO32-、CO32-、CH3COO-、NH4+、Na+等多种阴、阳离子.若向其中加入适量的Na2O2固体后,你认为原溶液中离子浓度基本保持不变的微粒有( )
| A. | 3种 | B. | 2种 | C. | 1种 | D. | 无,都有变化 |
17.下列说法中,正确的是( )
| A. | 在光照条件下,体积比为1:1的CH4和Cl2充分反应可以制取CH3Cl | |
| B. | 乙烯和苯都可与溴水发生加成反应 | |
| C. | 用新制氢氧化铜可以检验淀粉是否完全水解 | |
| D. | 分子式同为C3H7Cl,但沸点不同的分子共有两种 |
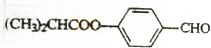 E的合成路线如下:
E的合成路线如下: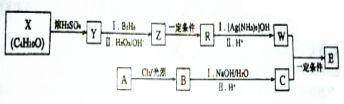
 .X→Y的反应类型是消去反应.
.X→Y的反应类型是消去反应.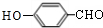 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$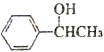 )为原料合成苯乙醛,设计合成路线:
)为原料合成苯乙醛,设计合成路线: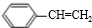 $\frac{Ⅰ.{B}_{2}{H}_{6}}{Ⅱ.{H}_{2}{O}_{2}/OH}$
$\frac{Ⅰ.{B}_{2}{H}_{6}}{Ⅱ.{H}_{2}{O}_{2}/OH}$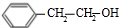 $\stackrel{Cu/△}{→}$
$\stackrel{Cu/△}{→}$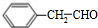 .
.