题目内容
标准状况下,m g气体X和n g气体Y所含分子数相同,以下说法错误的是
- A.X与Y两气体的相对分子质量之比为m:n
- B.同温同压下X与Y两气体的密度之比为n:m
- C.等质量气体X与Y所含分子数之比为n:m
- D.同温同压下,等体积的X与Y质量比为m:n
B
分析:m g气体X和n g气体Y所含分子数相同,根据V=n?Vm,则二者的物质的量相同,根据m=n?M可知两种气体的相对分子质量之比,同温同压下两种气体的密度之比等于相对分子质量之比,根据n= =
=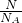 =
= 可知分子数与质量关系.
可知分子数与质量关系.
解答:m g气体X和n g气体Y所含分子数相同,根据V=n?Vm,则二者的物质的量相同,设物质的量为1mol,则
A、根据m=n?M可知两种气体的相对分子质量之比等于质量之比,为m:n,故A正确;
B、由n= 可知,
可知, ,在相同条件下气体的密度之比等于相对分子质量之比,为m:n,故B错误;
,在相同条件下气体的密度之比等于相对分子质量之比,为m:n,故B错误;
C、由n= =
=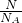 可知,等质量气体X与Y所含分子数与相对分子质量成反比,即为n:m,故C正确;
可知,等质量气体X与Y所含分子数与相对分子质量成反比,即为n:m,故C正确;
D、n= =
= 可知,同温同压下,等体积的X与Y质量之比等于相对分子质量之比,为m:n,故D正确.
可知,同温同压下,等体积的X与Y质量之比等于相对分子质量之比,为m:n,故D正确.
故选B.
点评:本题考查阿伏加德罗定律及推论,题目难度中等,注意物质的量与体积、密度、原子数目的计算公式的运用.
分析:m g气体X和n g气体Y所含分子数相同,根据V=n?Vm,则二者的物质的量相同,根据m=n?M可知两种气体的相对分子质量之比,同温同压下两种气体的密度之比等于相对分子质量之比,根据n=
 =
=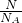 =
= 可知分子数与质量关系.
可知分子数与质量关系.解答:m g气体X和n g气体Y所含分子数相同,根据V=n?Vm,则二者的物质的量相同,设物质的量为1mol,则
A、根据m=n?M可知两种气体的相对分子质量之比等于质量之比,为m:n,故A正确;
B、由n=
 可知,
可知, ,在相同条件下气体的密度之比等于相对分子质量之比,为m:n,故B错误;
,在相同条件下气体的密度之比等于相对分子质量之比,为m:n,故B错误;C、由n=
 =
=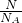 可知,等质量气体X与Y所含分子数与相对分子质量成反比,即为n:m,故C正确;
可知,等质量气体X与Y所含分子数与相对分子质量成反比,即为n:m,故C正确;D、n=
 =
= 可知,同温同压下,等体积的X与Y质量之比等于相对分子质量之比,为m:n,故D正确.
可知,同温同压下,等体积的X与Y质量之比等于相对分子质量之比,为m:n,故D正确.故选B.
点评:本题考查阿伏加德罗定律及推论,题目难度中等,注意物质的量与体积、密度、原子数目的计算公式的运用.

练习册系列答案
相关题目
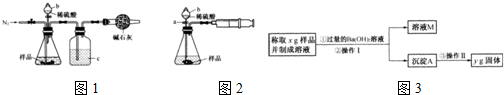
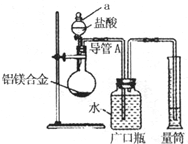 含镁3%~5%的铝镁合金是轮船制造、化工生产、机械制造等行业的重要材料.现有一块质量为m g的铝镁合金,欲测定其中镁的质量分数,几位同学设计了不同的实验方案.
含镁3%~5%的铝镁合金是轮船制造、化工生产、机械制造等行业的重要材料.现有一块质量为m g的铝镁合金,欲测定其中镁的质量分数,几位同学设计了不同的实验方案.