题目内容
某探究小组在实验室中
用铝土矿(主要成分为Al2O3,还含有Fe2O3、
SiO2)提取氧化铝。回答下列问题:
(1)在实验中需用1mol·L 的NaOH溶液480mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是 .
的NaOH溶液480mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是 .
在灼烧操作中用到下列仪器中的一种,其名称是 。
(2)写出步骤①中发生反应的离子方程式 。
(3)操作③中洗涤如何操作 。
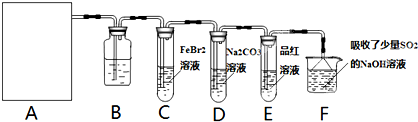
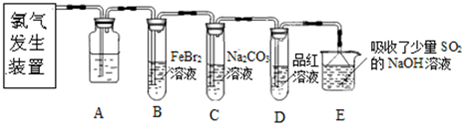
(4)甲同学在实验室中用下列装置制备CO2气体,并通人滤液B中制备Al(OH)3时,结果没有产生预期现象。
乙同学分析认为:甲同学通入CO2不足是导致实验失败的原因之一,你认为乙的分析是否合理? 。
若合理,请用离子方程式解释其原因 .
(若你认为不合理,该空不作答)
丙同学分析认为:甲同学通人的CO2中含有HCl气体,也是导致实验失败的原因,在实验中增加某装置可解决这个问题。请帮助丙同学画出该装置图,并注明试剂名称。

解析

练习册系列答案
相关题目




 的NaOH溶液480mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是 .
的NaOH溶液480mL,配制该溶液已有下列仪器:托盘天平(砝码)、胶头滴管、药匙、玻璃棒,还缺少的仪器是 .



