题目内容
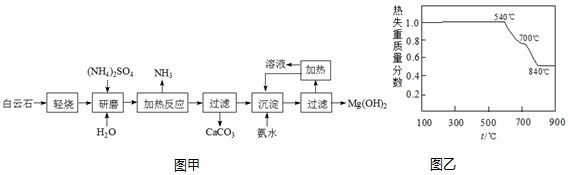
碱式碳酸铜[Cu2(OH)2CO3]是一种用途广泛的化工原料.工业上可用电子工业中刻蚀线路板的酸性废液(主要成分有FeCl3、CuCl2、FeCl2)制备,其制备过程如下:
查阅资料知,通过调节溶液的酸碱性可使Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
(1)氯酸钠的作用是 ;
(2)调节溶液A的pH范围为 ,可以选择的试剂是 .(填序号)
a.氨水 b.硫酸铜 c.氢氧化铜 d.碳酸铜
(3)反应B的温度要控制在60℃左右,且保持恒温,可采用的加热方法是 .
(4)已知滤液中含有碳酸氢钠,写出生成碱式碳酸铜的离子方程式: .

查阅资料知,通过调节溶液的酸碱性可使Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
(2)调节溶液A的pH范围为
a.氨水 b.硫酸铜 c.氢氧化铜 d.碳酸铜
(3)反应B的温度要控制在60℃左右,且保持恒温,可采用的加热方法是
(4)已知滤液中含有碳酸氢钠,写出生成碱式碳酸铜的离子方程式:
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:根据流程可知,废液中加入次氯酸钠将亚铁离子氧化成铁离子,然后用氢氧化铜或碳酸铜调节溶液的pH生成氢氧化铁除去铁离子,过滤后加入碳酸钠溶液生成碱式碳酸铜,过滤后得到碱式碳酸铜,
(1)亚铁离子不容易除去,需要加入次氯酸钠将亚铁离子氧化成铁离子,便于除去杂质;
(2)根据铁离子完全沉淀、氢氧化铜开始沉淀的pH确定溶液A的pH;
(3)根据反应温度需要控制在60℃左右分析加热方法;
(4)根据题中信息判断反应物为铜离子、碳酸根离子,反应产物为碱式碳酸铜和碳酸氢根离子,据此写出反应的离子方程式.
(1)亚铁离子不容易除去,需要加入次氯酸钠将亚铁离子氧化成铁离子,便于除去杂质;
(2)根据铁离子完全沉淀、氢氧化铜开始沉淀的pH确定溶液A的pH;
(3)根据反应温度需要控制在60℃左右分析加热方法;
(4)根据题中信息判断反应物为铜离子、碳酸根离子,反应产物为碱式碳酸铜和碳酸氢根离子,据此写出反应的离子方程式.
解答:
解:根据流程可知,制备碱式碳酸铜的方法为:废液中加入次氯酸钠将亚铁离子氧化成铁离子,然后用氢氧化铜或碳酸铜调节溶液的pH生成氢氧化铁除去铁离子,过滤后加入碳酸钠溶液生成碱式碳酸铜,过滤后得到碱式碳酸铜,
(1)由于沉淀氢氧化亚铁的pH大于沉淀氢氧化铁的pH,所以应该把亚铁离子氧化生成铁离子,然后再沉淀,所以氯酸钠的作用是将Fe2+氧化成Fe3+,
故答案为:将Fe2+氧化成Fe3+;
(2)根据表中数据可知,要沉淀氢氧化铁,而不沉淀氢氧化铜,则溶液的pH应该控制在3.7~6.0之间;
制备碱式碳酸铜,由于不能引入杂质,所以选择的试剂可以为氢氧化铜、氧化铜,故cd正确,
故答案为:3.7~6.0;cd;
(3)要控制在60℃左右,且保持恒温,可通过水浴加热的方法完成,
故答案为:水浴加热;
(4)铜离子、碳酸根离子和水反应生成碱式碳酸铜和碳酸氢根离子,反应的离子方程式为:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-,
故答案为:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-.
(1)由于沉淀氢氧化亚铁的pH大于沉淀氢氧化铁的pH,所以应该把亚铁离子氧化生成铁离子,然后再沉淀,所以氯酸钠的作用是将Fe2+氧化成Fe3+,
故答案为:将Fe2+氧化成Fe3+;
(2)根据表中数据可知,要沉淀氢氧化铁,而不沉淀氢氧化铜,则溶液的pH应该控制在3.7~6.0之间;
制备碱式碳酸铜,由于不能引入杂质,所以选择的试剂可以为氢氧化铜、氧化铜,故cd正确,
故答案为:3.7~6.0;cd;
(3)要控制在60℃左右,且保持恒温,可通过水浴加热的方法完成,
故答案为:水浴加热;
(4)铜离子、碳酸根离子和水反应生成碱式碳酸铜和碳酸氢根离子,反应的离子方程式为:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-,
故答案为:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-.
点评:本题考查通过碱式碳酸铜的制备,考查了物质实验方案的设计原则,题目难度中等,明确制备流程及反应原理为解答此类题关键,注意选用的除杂试剂既能够除去杂质,还不能引进新的杂质离子,试题侧重考查了学生的分析、理解能力及化学实验能力.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
下列各物质中物质的量最多的是(NA表示阿伏伽德罗常数)( )
| A、1 mol CO2 |
| B、标准状况下44.8 L H2 |
| C、3 NA 个水分子 |
| D、1 L 1 mol/L的硫酸钠溶液中所含的溶质 |
下列化学实验操作或事故处理方法不正确的是( )
| A、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 |
| C、酒精灯着火时可用湿布扑灭 |
| D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加浓硫酸 |