题目内容
17.下列说法不正确的是( )| A. | 钠和钾的合金具有导电性,可用于中子反应堆热交换剂 | |
| B. | 采用催化措施,将汽车尾气中的CO和NO转化为无害气体 | |
| C. | 信息产业中的光缆的主要成分是单质硅 | |
| D. | 水玻璃易溶于水,可用于生产黏合剂和防火剂 |
分析 A、钠钾合金为液态,作原子反应堆作热交换剂;
B、汽车尾气中的一氧化碳和一氧化氮在催化剂作用下反应生成无污染的气体二氧化碳和氮气;
C、光缆的主要成分是二氧化硅;
D、水玻璃是硅酸钠的水溶液,根据硅酸钠的性质来回答.
解答 解:A、钠钾合金为液态,具有导热性,可作快中子反应堆作热交换剂,故A错误;
B、汽车尾气中的一氧化碳和一氧化氮在催化剂作用下反应生成无污染的气体二氧化碳和氮气,采用催化措施,将汽车尾气中的CO和NO转化为无害气体,故B正确;
C、信息产业中的光缆的主要成分是二氧化硅,故C错误;
D、水玻璃是硅酸钠的水溶液,硅酸钠具有黏性,所以可作粘合剂;涂有硅酸钠溶液的木条加热时,水分蒸发后不易燃烧,所以可作防火剂,故D正确;
故选AC.
点评 本题侧重物质的性质以及应用知识的考查,注意知识的归纳和梳理是解体的关键,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.一定温度下,向2.0L恒容密闭容器中充入1.0mol A,经一段时间后反应A(g)?B(g)+C(g)达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(B)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 前50 s内B的平均反应速率v(B)=0.0032 mol•L-1•s-1 | |
| B. | 相同温度下,若达到平衡后向容器中继续充入A,则平衡向右移动,平衡常数增大 | |
| C. | 相同温度下,若起始时向容器中充入1.0 mol A、0.20 mol B和0.20 mol C,则达到平衡前v(正)>v(逆) | |
| D. | 若保持其他条件不变,升高温度,平衡时,平衡常数K=0.2 mol•L-1,则反应的△H<0 |
8.一定条件下的反应:PCl5(g)?PCl3(g)+Cl2(g)(正反应吸热)达到平衡后,下列情况使PCl5分解率降低的是 ( )
| A. | 温度、体积不变,充入氩气 | B. | 条件不变,对体系加热 | ||
| C. | 温度、体积不变,充入氯气 | D. | 温度不变,增大容器体积 |
12.在下列化合物:①CH3-CH3 ②CH2=CH2 ③ ④
④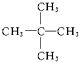 ⑤
⑤ ⑥CH3-CH═CH2 ⑦
⑥CH3-CH═CH2 ⑦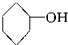 ⑧
⑧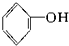 ⑨
⑨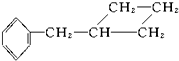 中,属于环状化合物的是③⑤⑦⑧⑨,属于脂环化合物的是⑤⑦,属于芳香化合物的是③⑧⑨,属于脂肪烃的是①②④⑥.
中,属于环状化合物的是③⑤⑦⑧⑨,属于脂环化合物的是⑤⑦,属于芳香化合物的是③⑧⑨,属于脂肪烃的是①②④⑥.
 ④
④ ⑤
⑤ ⑥CH3-CH═CH2 ⑦
⑥CH3-CH═CH2 ⑦ ⑧
⑧ ⑨
⑨ 中,属于环状化合物的是③⑤⑦⑧⑨,属于脂环化合物的是⑤⑦,属于芳香化合物的是③⑧⑨,属于脂肪烃的是①②④⑥.
中,属于环状化合物的是③⑤⑦⑧⑨,属于脂环化合物的是⑤⑦,属于芳香化合物的是③⑧⑨,属于脂肪烃的是①②④⑥.
2.相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ•mol-l.实验测得起始、平衡时的有关数据如下表:下列叙述正确的是( )
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
| SO2 | O2 | SO3 | Ar | ||
| 甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
| 乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2=78.8kJ |
| 丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
| A. | Q1>Q3>Q2=78.8kJ | |
| B. | 三个容器中反应的平衡常数均为K=2 | |
| C. | 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% | |
| D. | 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=$\frac{1}{5t}$ mol/(L•min) |
9.已知:在25℃时,向10mL 0.01mol•L-1NaCN溶液中逐滴加入0.01mol•L-1的盐酸,滴定曲线如图1所示,CN-、HCN浓度所占分数(α)随pH变化的关系如图2所示,下列表述正确的是( )
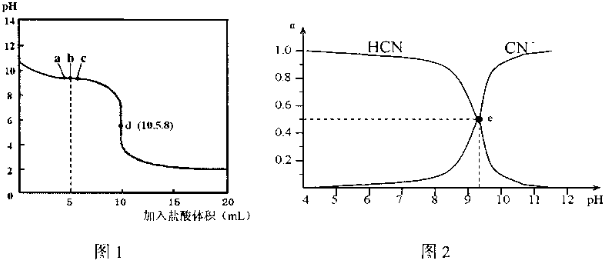

| A. | b点时,溶液中微粒浓度大小的关系:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+) | |
| B. | d点溶液存在的关系:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-) | |
| C. | 图2中的e点对应图1中的c点 | |
| D. | 在滴定过程中选用酚酞试剂比选用甲基橙试剂作指示剂误差更小 |
6.下列物质中同分异构体数目最多的是( )
| A. | C2H6O | B. | C3H8O | C. | C3H6BrCl | D. | C4H9Cl |
7.氮和硅均是自然界含量非常丰富的元素.
(1)氮化硅陶瓷是一种新型无机非金属材料,其化学式为Si3N4
(2)向大气中排放NOx可能导致的环境问题有酸雨、光化学烟雾、臭氧层破坏(任一点均可).(任答一点)用足量NaOH溶液能完全吸收NO2生成NaNO2、NaNO3和H2O2.试写出该反应的离子方程式:2NO2+2OH-═NO3-+NO2-+H2.
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料.工业上提纯硅有多种技术路线,其中一种工艺流程如图1:
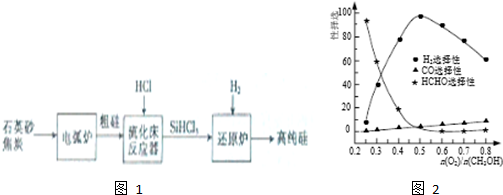
①电弧炉中发生的主要反应的化学方程式为SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑.
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和精馏(或蒸馏).
(4)“硅能源”有望成为二十一世纪的新能源.1mol硅完全燃烧能放出910kJ的热量,写出该反应的热化学方程式:Si(S)+O2(g)═SiO2(S)△H=-910KJ/mol;与“氢能源”比较“硅能源”具有的优点是产物不污染环境,储存、运输方便.
(5)工业上常利用甲醇部分氧化法制备氢气.在一定温度下以Ag/CeO2-SiO2为催化剂时原料气比例对反应选择性(选择性越大,表示生成的该物质越多)影响关系如图2所示.则当$\frac{n({O}_{2})}{n(C{H}_{3}OH)}$=0.25时,CH3OH与O2发生的主要反应方程式为2CH3OH+O2$→_{△}^{催化剂}$2HCHO+2H2O;当$\frac{n({O}_{2})}{n(C{H}_{3}OH)}$>0.5时,H2选择性下降的原因氧气过量,与氢气反应生成水.
(1)氮化硅陶瓷是一种新型无机非金属材料,其化学式为Si3N4
(2)向大气中排放NOx可能导致的环境问题有酸雨、光化学烟雾、臭氧层破坏(任一点均可).(任答一点)用足量NaOH溶液能完全吸收NO2生成NaNO2、NaNO3和H2O2.试写出该反应的离子方程式:2NO2+2OH-═NO3-+NO2-+H2.
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料.工业上提纯硅有多种技术路线,其中一种工艺流程如图1:

①电弧炉中发生的主要反应的化学方程式为SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑.
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和精馏(或蒸馏).
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
(5)工业上常利用甲醇部分氧化法制备氢气.在一定温度下以Ag/CeO2-SiO2为催化剂时原料气比例对反应选择性(选择性越大,表示生成的该物质越多)影响关系如图2所示.则当$\frac{n({O}_{2})}{n(C{H}_{3}OH)}$=0.25时,CH3OH与O2发生的主要反应方程式为2CH3OH+O2$→_{△}^{催化剂}$2HCHO+2H2O;当$\frac{n({O}_{2})}{n(C{H}_{3}OH)}$>0.5时,H2选择性下降的原因氧气过量,与氢气反应生成水.