题目内容
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

(1)操作①的名称是_____,操作②的名称是____。
(2)试剂a是_____(填化学式,下同),试剂b是____,固体B是_____。
(3)加入试剂a所发生反应的化学方程式为_______________________。加入试剂b所发生反应的化学方程式为_______________________。
【答案】溶解 过滤 K2CO3 HCl BaCl2 BaCl2 + K2CO3 = BaCO3↓ + 2KCl BaCO3 + 2HCl=BaCl2 + CO2↑+H2O
【解析】
分离KCl和BaCl2两种固体混合物,先溶于水配成溶液,然后加入过量K2CO3溶液使BaCl2完全转化为BaCO3沉淀,则试剂a为K2CO3溶液,过滤后BaCO3沉淀加入足量盐酸可生成BaCl2溶液,则试剂b为盐酸,在蒸发过程中过量的盐酸挥发,因此经蒸发、结晶、干燥后可得固体BaCl2;操作②所得滤液为KCl和K2CO3的混合物,应加入过量盐酸可得KCl溶液,经蒸发、结晶、干燥后可得固体KCl,据此进行分析。
(1)操作①是把KCl和BaCl2两种固体混合物溶于水,应为溶解;操作②是分离固体和液体的操作,应为过滤;
故答案为:溶解;过滤;
(2)固体溶解后加入过量K2CO3溶液使BaCl2转化为BaCO3沉淀,过滤后BaCO3沉淀加入足量的盐酸可生成BaCl2溶液,在蒸发过程中过量的盐酸挥发,经蒸发、结晶、干燥后可得固体BaCl2,故试剂a是K2CO3,试剂b是HCl,固体B是BaCl2;
故答案为:K2CO3;HCl;BaCl2;
(3)加入试剂a,K2CO3与BaCl2反应生成BaCO3沉淀和氯化钾,发生反应的化学方程式为:BaCl2 + K2CO3 = BaCO3↓ + 2KCl;加入试剂b,BaCO3与HCl生成二氧化碳、水和氯化钡,其反应的化学方程式为:BaCO3 + 2HCl=BaCl2 + CO2↑+H2O;
故答案为:BaCl2 + K2CO3 = BaCO3↓ + 2KCl;BaCO3 + 2HCl=BaCl2 + CO2↑+H2O。

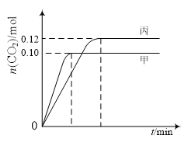
【题目】一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
容器 | 温度/℃ | 起始物质的量/mol | |
NO (g) | CO (g) | ||
甲 | T1 | 0.20 | 0.20 |
乙 | T1 | 0.30 | 0.30 |
丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的小
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D. T2℃时,若起始时向丙中充入0.06molN2和0.12 molCO2,则达平衡时N2的转化率大于40%