题目内容
5.在一定温度时,将1mol A和2mol B放入容积为5L的某密闭容器中发生如下反应:A(s)+2B(g)?C(g)+2D(g),经5min后测得容器内B的浓度减少了0.2mol•L-1.下列叙述不正确的是( )| A. | 在5 min内该反应用C表示的反应速率为0.02 mol•L-1•min-1 | |
| B. | 5 min时,容器内D的浓度为0.2 mol•L-1 | |
| C. | 当容器内压强保持恒定时,该可逆反应达到平衡状态 | |
| D. | 5 min时容器内气体总的物质的量为3 mol |
分析 经5min后测得容器内B的浓度减少了0.2mol•L-1,则消耗的B的物质的量为5L×0.2mol•L-1=1mol,则
A(s)+2B(g)?C(g)+2D(g)
起始:1mol 2mol 0 0
转化:0.5mol 1mol 0.5mol 1mol
平衡:0.5mol 1mol 0.5mol 1mol
以此可解答该题.
解答 解:经5min后测得容器内B的浓度减少了0.2mol•L-1,则消耗的B的物质的量为5L×0.2mol•L-1=1mol,则
A(s)+2B(g)?C(g)+2D(g)
起始:1mol 2mol 0 0
转化:0.5mol 1mol 0.5mol 1mol
平衡:0.5mol 1mol 0.5mol 1mol
A.在5min内该反应用C的浓度变化表示的反应速率为$\frac{\frac{0.5mol}{5L}}{5min}$=0.02mol•L-1•min-1,故A正确;
B.5min时,容器内D的浓度为$\frac{1mol}{5L}$=0.2mol•L-1,故B正确;
C.反应前后气体的体积不等,则当容器内压强保持恒定时,该可逆反应达到平衡状态,故C正确;
D.5min时容器内气体总的物质的量为1mol+0.5mol+1mol=2.5mol,故D错误.
故选D.
点评 本题考查化学平衡的计算,题目难度不大,注意根据三段式法计算较为直观,易错点为CD,注意A为固体的特征.

练习册系列答案
相关题目
15.实验室里用下列药品和仪器来制取纯净的无水氯化铜:
图中A、B、C、D、E、F的虚线部分表示玻璃管接口,接口的弯曲和伸长等部分未画出.根据要求填写下列各小题空白.
(1)如果所制得气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)
③接⑤接④接②接①接⑥;其中,②与④装置相连时,玻璃管接口(用装置中字母表示)应是接C.
(2)装置⑥中发生反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O.
(3)实验开始时,应首先检验装置的气密性;实验结束时,应先熄灭①处的酒精灯.
(4)在装置⑤的烧瓶中,发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2+2H2O
(5)待充分反应后,装置①的玻璃管中呈棕黄色.冷却后,将制得的产物配成溶液,溶液呈绿(或蓝绿)色.
(6)若反应中有71gCl2生成,则被氧化的HCl的物质的量为2mol,转移电子数为2NA.
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 | 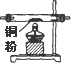 |  |  |  | 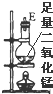 |  |
(1)如果所制得气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)
③接⑤接④接②接①接⑥;其中,②与④装置相连时,玻璃管接口(用装置中字母表示)应是接C.
(2)装置⑥中发生反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O.
(3)实验开始时,应首先检验装置的气密性;实验结束时,应先熄灭①处的酒精灯.
(4)在装置⑤的烧瓶中,发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2+2H2O
(5)待充分反应后,装置①的玻璃管中呈棕黄色.冷却后,将制得的产物配成溶液,溶液呈绿(或蓝绿)色.
(6)若反应中有71gCl2生成,则被氧化的HCl的物质的量为2mol,转移电子数为2NA.
16.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l);△H=-890.3kJ/mol,等质量的氢气和甲烷分别燃烧后,放出的热量之比约为( )
| A. | 1:3.4 | B. | 1:1.7 | C. | 2.6:1 | D. | 4.6:1 |
20.1.52g铜镁合金完全溶解于50mL 密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1 120mL (标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀,下列说法不正确的是( )
| A. | 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L | |
| C. | NO2和N2O4 的混合气体中,NO2的体积分数是80% | |
| D. | 该合金中铜与镁的物质的量之比是2:1 |
14.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol Cl2参加反应,转移的电子数目一定为0.2NA | |
| B. | 1.4g聚乙烯中含C-H数目为0.2NA | |
| C. | 标准状况下,5.6L甲醇中含有的分子数目为0.2NA | |
| D. | 常温下,pH=13的NaOH溶液中含OH-的数目为0.1NAA |
15.在高温下用一氧化碳还原mg四氧化三铁得到ng铁.已知氧的相对原子质量为16,则铁的相对原子质量为( )
| A. | $\frac{21n}{m-n}$ | B. | $\frac{64n}{3(m-n)}$ | C. | $\frac{m-n}{32n}$ | D. | $\frac{24n}{m-n}$ |
 )相同,且同时符合下列两个条件:①苯环上带有两个取代基,②有一个硝基直接连在苯环上,则符合此条件的同分异构体数目是( )
)相同,且同时符合下列两个条件:①苯环上带有两个取代基,②有一个硝基直接连在苯环上,则符合此条件的同分异构体数目是( )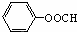 (写出结构简式).
(写出结构简式). +3NaOH→C17H35COONa+
+3NaOH→C17H35COONa+ .
.