题目内容
10.乳酸橙花酯是一种食用香料,其结构如图所示.下列关于该物质的说法不正确的是( )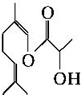
| A. | 1 mol该化合物最多可与2 mol H2反应 | |
| B. | 该化合物能与乳酸发生酯化反应 | |
| C. | 该化合物能与氢氧化钠溶液、溴水反应 | |
| D. | 该化合物的同分异构体可能为芳香族化合物 |
分析 由有机物的结构简式可知,分子中含碳碳双键、-COOC-,结合烯烃和酯的性质来解答.
解答 解:A.1 mol乳酸橙花酯中含有2 mol碳碳双键,故最多可与2 mol H2 反应,故A正确;
B.乳酸橙花酯中含有羟基,故可与乳酸发生酯化反应,故B正确;
C.乳酸橙花酯中含有酯基和碳碳双键,故可分别与氢氧化钠溶液和溴水反应,故C正确;
D.有机物含3个双键,不报核对为3,而苯环不饱和对为4,该化合物的同分异构体不可能为芳香族化合物,故D错误.
故选D.
点评 本题考查有机物的结构与性质,为高考常见题型,把握常见有机物的官能团为解答的关键,熟悉烯烃、酯的性质即可解答,题目难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
20.下列关于Fe( OH)3胶体的说法中,不正确的是( )
| A. | 分散质粒子直径在10-9~l0-7m之间 | B. | 是一种纯净物 | ||
| C. | 具有丁达尔效应 | D. | 具有净水作用 |
18.已知短周期元素的离子aA3+、bB+、cC2-、dD-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数:c>b | B. | 离子的还原性:C2-<D- | ||
| C. | 氢化物的稳定性:H2C>HD | D. | 离子半径:B+>A3+ |
5.下表是第二、三周期元素性质的部分数据:
(1)以上9种元素中,金属性最强的是Na,非金属性最强的是F.(填元素符号)
(2)②和⑨形成的化合物是共价化合物(填“离子化合物”或“共价化合物”).
(3)①、②与氢元素能形成一种常见的有机物,这种物质常用于医疗消毒.在空气中,将灼热的铜丝插入该物质,反应的化学方程式为2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O
(4)16g铜金合金与足量的某浓度的⑧的最高价氧化物对应的水化物反应,将产生的气体与1.12L(标准状况)O2混合,通入水中,气体恰好完全被吸收,重新生成⑧的最高价氧化物对应的水化物.该合金中铜的质量分数为40%.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 原子半径/10-10 m | 0.74 | 0.77 | 1.52 | 1.02 | 1.10 | 0.71 | 1.86 | 0.75 | 0.99 |
| 最高化合价 | - | +4 | +1 | +6 | +5 | - | +1 | +5 | +7 |
| 最低化合价 | -2 | -4 | - | -2 | -3 | -1 | - | -3 | -1 |
(2)②和⑨形成的化合物是共价化合物(填“离子化合物”或“共价化合物”).
(3)①、②与氢元素能形成一种常见的有机物,这种物质常用于医疗消毒.在空气中,将灼热的铜丝插入该物质,反应的化学方程式为2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O
(4)16g铜金合金与足量的某浓度的⑧的最高价氧化物对应的水化物反应,将产生的气体与1.12L(标准状况)O2混合,通入水中,气体恰好完全被吸收,重新生成⑧的最高价氧化物对应的水化物.该合金中铜的质量分数为40%.
15.下列说法中错误的是( )
| A. | 若XY4分子中X原子处于正四面体的中心,则XY4分子为非极性分子 | |
| B. | C2H5OH与C2H5Br相比,前者的相对分子质量远小于后者,而沸点却远高于后者,其原因是前者的分子间存在氢键 | |
| C. | CO2与SiO2晶体熔化时,所克服的微粒间相互作用不同 | |
| D. | 短周期元素离子aXn-和bYm-具有相同的电子层结构,若a>b,则n>m |
20.设NA表示阿伏伽德罗常数的值,则下列说法正确的是( )
| A. | NA个氢分子的质量与氢气的摩尔质量在数值上相等 | |
| B. | NA个氢气分子和NA个氯气分子的质量之比1:1 | |
| C. | 16g氧气所含氧分子数目为NA | |
| D. | 44gCO2与44gCO所含的分子数目均为NA |
 如图是一个用铂丝作电极,电解Na2SO4溶液的装置,电解液中加有酚酞.闭合开关,电解一段时间后发现:a、b试管中产生气体的体积比为2:1.
如图是一个用铂丝作电极,电解Na2SO4溶液的装置,电解液中加有酚酞.闭合开关,电解一段时间后发现:a、b试管中产生气体的体积比为2:1.
 .
.