��Ŀ����
CO�Ǻϳ����ء������ԭ�ϡ�
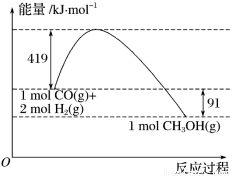
��1����l00kPa��TK�£����ȶ���������1mol��������ʱ��Ϊ��������TKʱ�ı�Ħ�������ʣ��÷��š�H0��ʾ����֪ʯī��һ����̼��ȼ���ȷֱ�Ϊ393��5kJ/mol��283��0 kJ/mol����CO(g)�ġ�H0=________��
��2���ϳ����صķ�Ӧ��2NH3(g)+CO (g)=CO(NH2)2(g)+H2(g) ��H = - 81��0kJ/mol��T��ʱ�������Ϊ2L�ĺ����ܱ������У���2 mol��NH3��1mol CO��Ϸ�Ӧ��5 minʱ��NH3��ת����Ϊ80%����0��5minƽ����Ӧ����Ϊv(CO)= ��

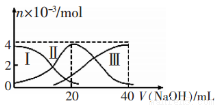
��K1 126.5���>����< ���������ж������� �������ֺ��º��������������ʵ���֮��Ϊ3 mol��NH3��CO�Բ�ͬ�İ�̼�Ƚ��з�Ӧ�������ͼ��ʾ��
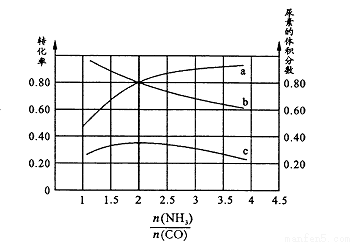
��ͼ��c��ʾƽ����ϵ�����ص������������a��ʾ________��ת���ʡ�
�ڵ�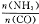 = ʱ�����غ������ʱ�����ڸ÷��������������Ӧ��������ʹƽ�������ƶ��Ĵ�ʩ�� ��дһ�֣���
= ʱ�����غ������ʱ�����ڸ÷��������������Ӧ��������ʹƽ�������ƶ��Ĵ�ʩ�� ��дһ�֣���
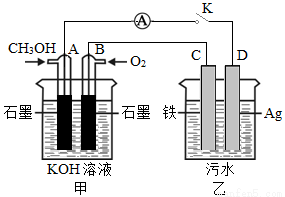
��3��ͨ���˹�������ÿɽ�COת����HCOOH����֪�����£�Ũ�Ⱦ�Ϊ0.1 mol��L��HCOOH��HCOONa�����ҺpH =3.7����HCOOH�ĵ��볣��Ka= ����֪lg2=0.3�����õ绯ѧ������HCOOH��ˮ����ɵ���Ⱦ����ԭ���ǵ��CoSO4��ϡ�����HCOOH�����Һ���õ�������Co3+��HCOOH������CO2��
��Co3+����HCOOH�����ӷ���ʽΪ ��
�ں�������仯�����ǰ��Co2+��Ũ�Ƚ� �����������С�����䡱����


 xC(g) ��H<0��B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ1����ƽ�����t1��t2��t3��t4ʱ��ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2��
xC(g) ��H<0��B��C�����ʵ�����ʱ��仯�Ĺ�ϵ��ͼ1����ƽ�����t1��t2��t3��t4ʱ��ֻ�ı���һ���������淴Ӧ������ʱ��仯�Ĺ�ϵ��ͼ2��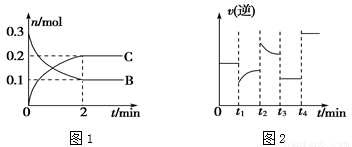
 CH3OH(g)+H2O(g) ��H��0����˵���÷�Ӧ�Ѵ�ƽ��״̬���ǣ� ��
CH3OH(g)+H2O(g) ��H��0����˵���÷�Ӧ�Ѵ�ƽ��״̬���ǣ� �� ol H2��ͬʱ����0.4mol H2O
ol H2��ͬʱ����0.4mol H2O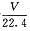 NA
NA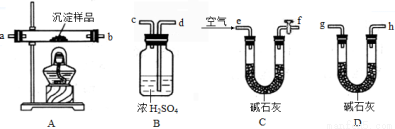
 CH3OH(g)��
CH3OH(g)��