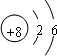题目内容
有A、B、C、D、E五种短周期元素,它们的核电荷数依次增大.A、D 都能分别与B按原子个数比为1:1 或2:1形成化合物;AC可与EB2反应生成A2B与气态物质EC4;E的M层电子数是K层电子数的2倍.
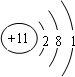
(1)画出E的原子结构示意图
 ;写出电子式D2B2
;写出电子式D2B2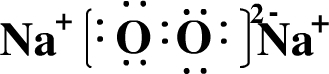
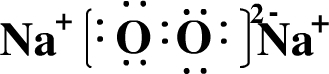 ;写出化学式EC4
;写出化学式EC4
(2)比较EB2与EC4的沸点高低(填化学式)
(3)用电子式表示化合物DC的形成过程
 .
.
(1)画出E的原子结构示意图


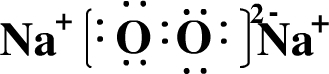
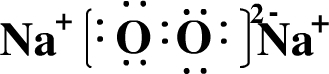
SiF4
SiF4
.(2)比较EB2与EC4的沸点高低(填化学式)
SiO2
SiO2
>SiF4
SiF4
.(3)用电子式表示化合物DC的形成过程


分析:A、B、C、D、E五种短周期元素,它们的核电荷数依次增大,A、D 都能分别与B按原子个数比为1:1 或2:1形成化合物,则A为H,B为O,D为Na;E的M层电子数是K层电子数的2倍,则E的质子数为14,即E为Si;AC可与EB2反应生成A2B与气态物质EC4,该反应为4HF+SiO2═2H2O+SiF4↑,则C为F,然后利用元素及其单质、化合物的性质来解答.
解答:解:A、B、C、D、E五种短周期元素,它们的核电荷数依次增大,A、D 都能分别与B按原子个数比为1:1 或2:1形成化合物,则A为H,B为O,D为Na;E的M层电子数是K层电子数的2倍,则E的质子数为14,即E为Si;AC可与EB2反应生成A2B与气态物质EC4,该反应为4HF+SiO2═2H2O+SiF4↑,则C为F,
(1)E为Si,质子数为14,最外层电子数为4,原子结构示意图为 ,D2B2为Na2O2,电子式为
,D2B2为Na2O2,电子式为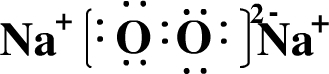 ,
,
EC4为SiF4,故答案为: ;
;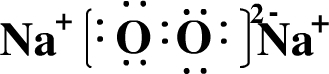 ;SiF4;
;SiF4;
(2)SiO2为原子晶体,熔沸点较高,SiF4为分子晶体,熔沸点较低,沸点SiO2>SiF4,故答案为:SiO2;SiF4;
(3)NaF为离子化合物,形成过程为 ,故答案为:
,故答案为: .
.
(1)E为Si,质子数为14,最外层电子数为4,原子结构示意图为
 ,D2B2为Na2O2,电子式为
,D2B2为Na2O2,电子式为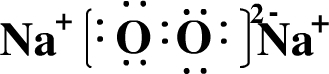 ,
,EC4为SiF4,故答案为:
 ;
;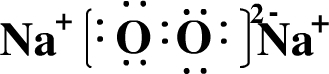 ;SiF4;
;SiF4;(2)SiO2为原子晶体,熔沸点较高,SiF4为分子晶体,熔沸点较低,沸点SiO2>SiF4,故答案为:SiO2;SiF4;
(3)NaF为离子化合物,形成过程为
 ,故答案为:
,故答案为: .
.点评:本题考查原子结构、元素周期律、元素的性质,熟悉元素形成的常见化合物是解答本题的关键,注意二氧化硅的特性来解答.

练习册系列答案
相关题目