题目内容
下列各反应的能量变化分别用如下形式的示意图表示,其中正确的是( )
A、 化石燃料的燃烧 |
B、 植物的光合作用 |
C、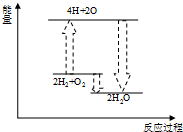 氢气与氧气反应 |
D、 氢气与氯气反应 |
考点:常见的能量转化形式,吸热反应和放热反应
专题:化学反应中的能量变化
分析:A.化石燃料燃烧是放热反应;
B.植物光合作用是绿色植物把二氧化碳和水合成有机物,释放氧气,同时把光能转变成化学能储存在合成的有机物中的过程;
C.氢气和氧气的反应过程中断裂化学键吸收能量,形成化学键放出能量,放出的能量大于吸收的能量,反应过程中放热;
D.氢气和氯气的反应过程中拆化学键吸收能量,形成化学键放出能量,反应放出的能量高于吸收的能量,反应是放热反应.
B.植物光合作用是绿色植物把二氧化碳和水合成有机物,释放氧气,同时把光能转变成化学能储存在合成的有机物中的过程;
C.氢气和氧气的反应过程中断裂化学键吸收能量,形成化学键放出能量,放出的能量大于吸收的能量,反应过程中放热;
D.氢气和氯气的反应过程中拆化学键吸收能量,形成化学键放出能量,反应放出的能量高于吸收的能量,反应是放热反应.
解答:
解:A、化石燃料燃烧是放热反应,反应物的能量高于生成物能量,图象表示的是吸热反应,与化石燃料的燃烧不符合,故A错误;
B.植物光合作用是绿色植物把二氧化碳和水合成有机物,释放氧气,同时把光能转变成化学能储存在合成的有机物中的过程,反应物能量低于生成物,图象中反应物能量高于生成物能量,与光合作用的能量变化不相符,故B错误;
C.氢气和氧气的反应过程为放热反应,反应物能量高于生成物,图象符合氢气与氧气反应中的能量变化,故C正确;
D.氢气和氯气的反应过程中拆化学键吸收能量,形成化学键放出能量,反应放出的能量高于吸收的能量,反应是放热反应,反应物能量高于生成物,图象不符合,故D错误;
故选C.
B.植物光合作用是绿色植物把二氧化碳和水合成有机物,释放氧气,同时把光能转变成化学能储存在合成的有机物中的过程,反应物能量低于生成物,图象中反应物能量高于生成物能量,与光合作用的能量变化不相符,故B错误;
C.氢气和氧气的反应过程为放热反应,反应物能量高于生成物,图象符合氢气与氧气反应中的能量变化,故C正确;
D.氢气和氯气的反应过程中拆化学键吸收能量,形成化学键放出能量,反应放出的能量高于吸收的能量,反应是放热反应,反应物能量高于生成物,图象不符合,故D错误;
故选C.
点评:本题考查了化学反应能量变化的特征和反应实质判断,题目难度不大,掌握能量变化和反应前后能量守恒是解题关键,注意光合作用的实质.

练习册系列答案
相关题目
下列化学用语书写正确的是( )
A、氯原子的结构示意图: |
B、CO2的比例模型: |
C、氯化氢的电子式: |
| D、二氧化硅分子式:SiO2 |
下列说法中正确的是( )
| A、用完的电池可以随意地丢弃 |
| B、增加炼铁高炉的高度可以降低尾气中CO的含量 |
| C、加入正催化剂是能大大提高化学反应速率 |
| D、把煤粉碎了再燃烧不可以提高煤的燃烧效率 |
钛被认为是21世纪的重要金属材料,已知某种钛原子的质子数为22,中子数为26,则该钛原子的核外电子数为( )
| A、4 | B、22 | C、26 | D、48 |
在一定条件下,把一定量NH3充入容积固定的密闭容器中,发生反应2NH3 (g)?3H2(g)+N2(g).达到平衡时,如果保持温度不变,增加N2的浓度.下列说法正确的是( )
| A、平衡向正反应方向移动 |
| B、化学平衡常数不变 |
| C、化学平衡常数增大 |
| D、化学平衡常数减小 |
下列表示物质结构的化学用语正确的是( )
| A、HT、D2互为同素异形体 |
B、HF的电子式: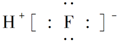 |
C、NH4Cl的电子式: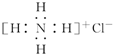 |
D、CaC2的电子式: |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、16 g甲烷分子中含有共价键的数目为2NA |
| B、常温常压下,30g葡萄糖含有的氧原子数为NA |
| C、0.1mol/L的AlCl3溶液中含有的氯离子数为0.3NA |
| D、25℃时,1L 0.1mol/L的CH3COOH溶液中的H+数为0.1NA |
下列有关电解质溶液中微粒的物质的量浓度关系不正确的是( )
| A、在0.1 mol?L-1 NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| B、在0.1 mol?L-1 Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| C、向0.2 mol?L-1 NaHCO3溶液中加入等体积0.1 mol?L-1 NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol?L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |