题目内容
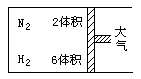
在一定温度下,把2体积N2和6体积H2通入一带活塞的体积可变的容器中,活塞的一端与大气相通(如图所示).容器中发生以下反应:N2+3H2![]() 2NH3(正反应放热),若达到平衡后,测得混合气体的体积为7体积,据此回答下列问题:
2NH3(正反应放热),若达到平衡后,测得混合气体的体积为7体积,据此回答下列问题:
(1)保持上述反应温度不变,设a,b,c分别代表初始加入的N2,H2和NH3的体积,如果反应达到平衡时,各物质的百分含量以及总体积与上述平衡完全相同,那么:
①若a=1,c=2,则b=________,在此情况下,反应起始时将向________(填“正反应”、“逆反应”)方向进行.
②若规定起始时反应向逆方向进行,则c的范围是________.
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是________,其理由是________.
答案:
解析:
提示:
解析:
|
(1)①3,逆反应,②1<c≤4;(2)降温,正反应为放热反应,降温平衡正向移动,最终体积可减小至6.5体积 【巧解导析】该反应是在 T,p一定下进行的反应.只要v(H2)∶v(N2)=3∶1就可达到同一平衡状态.2体积NH3与1体积N2和3体积H2相当,则b=3.因反应前为8体积,反应后为7体积,差量为1体积,由差量法可求出平衡时NH3为1体积.现c=2,NH3必须减小,所以平衡将向逆反应方向进行.若需让反应向逆反应方向进行,则氨的体积必须大于1.因1体积N2、3体积H2相当于2体积NH3,所以c的最大值为4,则c的范围是1<c≤4.(2)6.5<7,上述平衡应向体积缩小方向移动,因压强为一定值,故只有采取降温措施才能使平衡正向移动. |
提示:
|
【巧解点悟】解题关键点: T,p一定,达到平衡时各组分百分含量和体积完全相同,实际上相当于T,V一定,要求转化成相同起始物时,投料相等.易错点:不能将平衡状态和起始状态进行比较而判断反应方向和c的取值. |

练习册系列答案
相关题目
 (2011?泰州二模)能源、材料和信息是现代社会的三大“支柱”.
(2011?泰州二模)能源、材料和信息是现代社会的三大“支柱”.
 (2012?唐山二模)【化学--选修物质结构与性质】
(2012?唐山二模)【化学--选修物质结构与性质】
 水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。