题目内容
从键能角度来看,化学反应的本质是旧键断开,新键形成的过程,断开化学键要 (填“吸收”或“释放”,下同)能量.形成化学键要 能量;从能量角度来看,物质都储存化学能,若反应物的总能量低于生成物的总能量,则该反应要 能量.
考点:化学反应中能量转化的原因
专题:化学反应中的能量变化
分析:断开旧的化学键需要吸收能量,形成新的化学键会放出能量,若断开化学键吸收的能量小于形成化学键放出的能量,该反应为放热反应;若断开化学键吸收的能量大于形成化学键放出的能量,该反应为吸热反应;
从物质含有的能量角度分析,若反应物总能量高于生成物总能量,则为放热反应,若反应物总能量小于生成物总能量,则该反应为吸热反应.
从物质含有的能量角度分析,若反应物总能量高于生成物总能量,则为放热反应,若反应物总能量小于生成物总能量,则该反应为吸热反应.
解答:
解:化学反应的本质是化学键的断裂与形成,化学反应中能量变化的微观表现为:断开化学键需要吸收能量,形成新的化学键会放出能量;
从能量角度来看,物质都储存化学能,若反应物总能量高于生成物总能量,则为放热反应;若反应物的总能量低于生成物的总能量,则该反应要吸收能量,
答案为:放出;吸收,吸收.
从能量角度来看,物质都储存化学能,若反应物总能量高于生成物总能量,则为放热反应;若反应物的总能量低于生成物的总能量,则该反应要吸收能量,
答案为:放出;吸收,吸收.
点评:本题考查了化学反应与能量变化,试题侧重了基础知识的考查,题目难度不大,注意掌握化学反应与能量变化的关系,能够从化学键的断裂与形成、反应物与生成物总能量等不同角度分析化学反应中的能量变化.

练习册系列答案
相关题目
下列结构式从成键情况看不合理的是( )
A、 |
B、 |
C、 |
D、 |
下列判断不正确的是( )
| A、非金属性:F>O>S |
| B、稳定性:SiH4>PH3>H2S |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
下列卤代烃,在一定条件下,能发生消去反应的是( )
| A、CH3Cl |
| B、CH3-CHBr-CH3 |
C、 |
D、 |
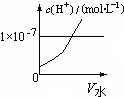



 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.