��Ŀ����
ѧϰԪ�������ɺ�ij�о���ѧϰС���ͬѧ�ǶԵ������ڹ���Ԫ�ص������������Ũ�����Ȥ������֪�������̶�����ش��ֽ�֪ʶ�Ļ����ϣ����뵽������������ͭ���������ȶ�����صķֽ��Ƿ��д����ã��Դ����ǽ�����ʵ���о��������Ҫ��������в���ʵ�鱨�棺
��1���������ƣ�______��
��2��ʵ���������Լ���
ʵ�������������е�����̨������Ƥ���ĵ��ܡ�����װ�á�����װ�á�������ƽ��ҩ�ס�______�ȣ�
ʵ���Լ����������̡�������������ͭ���������������
��3��ʵ�鲽�裺��
��4��ʵ�����ݣ�
| ʵ�� ��� | KClO3/g | ������ | ��������/mL �������㵽����� | ��ʱ/s | ||
| ��ѧʽ | ����/g | ���� | ||||
| 1 | 0.60 | - | - | - | 10 | 480 |
| 2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.60 | Cr2O3 | 0.20 | 90% | 67.2 | 188.3 |
����������ĻطŹ����У�Ҫ���еIJ������ܽ⡢______��ϴ�ӡ�______��������
��ʵ����3��ʵ����KClO3�ķֽ���Ϊ______������һλС������
���ں�Cr2O3���о�ʵ��ʱ�������д̼�����ζ�����������ͬʱ��ɫ�Ļ���������ٻ�ɫ���ô̼�����ζ��������______������______��ֽ���飮�����쳣���������ԭ����______��
��6��ʵ�����______��
��2���Ը���ʵ��Ҫ�ⶨʱ�䣬����Ӧ����������з�Ӧ�����ͼ���������
��5����CuO��Fe2O3��Cr2O3��������ˮ�����Ի�����Ҫ�ܽ⡢ϴ�ӡ����ˡ����������
���ȸ���n=
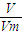 �������������ʵ������ٸ�������غ������Ĺ�ϵʽ��������ص����ʵ���������m=nM���㷴Ӧ������ص��������ټ���ֽ�����������������ص�����֮�ȼ��ɣ�
�������������ʵ������ٸ�������غ������Ĺ�ϵʽ��������ص����ʵ���������m=nM���㷴Ӧ������ص��������ټ���ֽ�����������������ص�����֮�ȼ��ɣ��۸���Ԫ���غ㼰�����ж�����������������ԣ���ʹʪ��ĵ��۵⻯�ر�����
��6������ͼ���л��յ������P��ʱ������������ȽϷ�����
����⣺��1����ʵ���Ŀ����̽��CuO��Fe2O3��Cr2O3�ȶ�����ص����ȷֽ���û�д����ã��������������Ϊ̽��CuO��Fe2O3��Cr2O3�ȶ�����ص����ȷֽⷴӦ�Ĵ����ã�
�ʴ�Ϊ��̽��������������ͭ���������ȶ�����ط����Ƿ��д����ã�
��2���Ը���ʵ��Ҫ�ⶨʱ�䣬����Ӧ����������з�Ӧ�����ͼ����������ʴ�Ϊ���Թܡ��ƾ��ơ������
��5����CuO��Fe2O3��Cr2O3��������ˮ�����Ի�����Ҫ�ܽ⡢ϴ�ӡ����ˡ����������
�ʴ�Ϊ�����ˡ����
���������������ʵ���Ϊn=
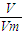 =
=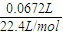 =0.003mol��
=0.003mol��2KCl3
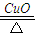 2KCl+3O2��
2KCl+3O2��2mol 3mol
0.002mol 0.003mol
���Է�Ӧ������ص����ʵ���Ϊ 0.002mol������Ϊm=nM=0.002mol×122.5g/mol=0.245g��
������ֽ���Ϊ
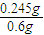 ×100%=40.8%��
×100%=40.8%���ʴ�Ϊ��40.8%��
����Cr2O3���о�ʵ��ʱ�������д̼�����ζ�����������ͬʱ��ɫ�Ļ���������ٻ�ɫ����CrԪ�صĻ��ϼ����ߣ�ClԪ�صĻ��ϼ۽��ͣ��������������������������ԭ��Ӧ�������������仯ѧʽΪCl2��������ʹʪ��ĵ��۵⻯����ֽ�����������ʹ��ʪ��ĵ��۵⻯����ֽ����������
�ʴ�Ϊ��Cl2��ʪ��ĵ��۵⻯�أ�KClO3��Cr2O3������������ԭ��Ӧ��
��6������ͼ���л��յ������P��ʱ������CuO��Cr2O3 ��������̱Ƚϣ���ʱ�ϳ���Cr2O3 �Ļ��������쳣���Ȼ����Ͷ������̵Ĵ����������
�ʴ�Ϊ��Fe2O3��CuO�ܶ�KC1O�ֽ�������ã�
���������⿼�黯ѧ��Ӧ����Ӱ������أ�̽�������Ի�ѧ��Ӧ���ʵ�Ӱ�켰��Ч����ע��ʵ����̼�ʵ�������ۣ��ܹ��ϺõĿ���ѧ���ۺ�Ӧ��֪ʶ��������

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�ѧϰԪ�������ɺ�ij�о���ѧϰС���ͬѧ�ǶԵ������ڹ���Ԫ�ص������������Ũ�����Ȥ������֪�������̶�����ش��ֽ�֪ʶ�Ļ����ϣ����뵽������������ͭ���������ȶ�����صķֽ��Ƿ��д����ã��Դ����ǽ�����ʵ���о���
�����Ҫ��������в���ʵ�鱨�棺
��1���������ƣ� ��
��2��ʵ���������Լ���
ʵ�������������е�����̨������Ƥ���ĵ��ܡ�����װ�á�����װ�á�������ƽ��ҩ�ס� �ȡ�
ʵ���Լ����������̡�������������ͭ���������������
��3��ʵ�鲽�裺��
��4��ʵ�����ݣ�
| ʵ�� ��� | KC1O3/g | ������ | ��������/mL �������㵽����� | ��ʱ/s | ||
| ��ѧʽ | ����/g | ���� | ||||
| 1 | 0.60 | �D | �D | �D | 10 | 480 |
| 2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.60 | Cr2O3 | 0.20 | 90% | 67.2 | 188.3 |
��5��ʵ�����ۣ�
����������ĻطŹ����У�Ҫ���еIJ������ܽ⡢ ��ϴ�ӡ� ��������
��ʵ����3��ʵ����KC1O3�ķֽ���Ϊ ������һλС������
���ں�Cr2O3���о�ʵ��ʱ�������д̼�����ζ�����������ͬʱ��ɫ�Ļ���������ٻ�ɫ���ô̼�����ζ�������� ������ ��ֽ���顣�����쳣���������ԭ���� ��
��6��ʵ����� ��
(08��ׯ����)ѧϰԪ�������ɺ�ij�о���ѧϰС���ͬѧ�ǶԵ������ڹ���Ԫ�ص������������Ũ�����Ȥ������֪�������̶�����ش��ֽ�֪ʶ�Ļ����ϣ����뵽������������ͭ���������ȶ�����صķֽ��Ƿ��д����ã��Դ����ǽ�����ʵ���о���
�����Ҫ��������в���ʵ�鱨�棺
��1���������ƣ� ��
��2��ʵ���������Լ���
ʵ�������������е�����̨������Ƥ���ĵ��ܡ�����װ�á�����װ�á�������ƽ��ҩ�ס��ȡ�
ʵ���Լ����������̡�������������ͭ���������������
��3��ʵ�鲽�裺��
��4��ʵ�����ݣ�
ʵ�� ��� | KC1O3/g | ������ | ��������/mL �������㵽����� | ��ʱ/s | ||
��ѧʽ | ����/g | ���� | ||||
1 | 0.60 | �D | �D | �D | 10 | 480 |
2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
5 | 0.60 | Cr2O3 | 0.20 | 90% | 67.2 | 188.3 |
��5��ʵ�����ۣ�
����������ĻطŹ����У�Ҫ���еIJ������ܽ⡢ ��ϴ�ӡ� ��������
��ʵ����3��ʵ����KC1O3�ķֽ���Ϊ ������һλС������
���ں�Cr2O3���о�ʵ��ʱ�������д̼�����ζ�����������ͬʱ��ɫ�Ļ���������ٻ�ɫ���ô̼�����ζ�������� ������ ��ֽ���顣�����쳣���������ԭ���� ��
��6��ʵ����� ��