题目内容
下列物质中既能跟稀H2SO4反应, 又能跟氢氧化钠溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al
| A.③④ | B.②③④ | C.①③④ | D.全部 |
D
解析试题分析:①NaHCO3属于弱酸酸式盐,既能与硫酸反应,生成CO2气体,又能与氢氧化钠反应,生成碳酸钠,故①正确;②Al2O3属于两性氧化物,既能与硫酸反应,生成Al3+离子,又能与氢氧化钠反应生成AlO2-离子,故②正确;③Al(OH)3 属于两性氢氧化物,既能与酸反应,生成Al3+离子,又能与碱反应生成AlO2-离子,故③正确;④金属铝与硫酸反应生成Al3+和氢气,与氢氧化钠反应生成AlO2-和氢气,故④正确。
考点:两性氧化物和两性氢氧化物;铝的化学性质。

 阅读快车系列答案
阅读快车系列答案钠与水反应的现象与钠的下列性质无关的是
| A.钠的熔点较低 | B.钠的密度小于水 |
| C.钠的硬度较小 | D.钠的还原性强 |
将ag镁铝合金投入到x mL 2mol/L的盐酸中,金属完全溶解后,再加入y mL 1mol/L的氢氧化钠溶液,得到的沉淀量最大,质量为 g。下列说法不正确的是
g。下列说法不正确的是
A.镁铝合金与盐酸反应转移电子总数为 |
B.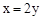 |
C.沉淀是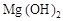 和 和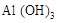 的混合物 的混合物 |
| D.1.2>a>0.9 |
在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是( )
| A.原溶液中n(Mg2+)∶n(Al3+)=10∶1 |
| B.原溶液的c(H+)=0.8 mol/L |
| C.x与y的差值为0.01 mol |
| D.原溶液中c(Cl-)=0.66mol/L |
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100 mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42- 的物质的量浓度为6 mol·L-1,则此溶液最多溶解铁粉的质量为( )
| A.5.6 g | B.11.2 g | C.22.4 g | D.33.6 g |
某些补铁剂的成分中含有硫酸亚铁,长期放置会因氧化而变质。检验硫酸亚铁是否变质的试剂是
| A.稀盐酸 | B.KSCN溶液 | C.氯水 | D.铁粉 |
有Al、CuO、Fe2O3组成的混合物共10.0 g,放入500 mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250 mL 2.0 mol/L的NaOH溶液时,得到的沉淀最多。上述盐酸溶液的浓度为( )
| A.0.5 mol/L | B.3.0 mol/L |
| C.2.0 mol/L | D.1.0 mol/L |
Al、Fe、Cu都是重要的金属元素。下列说法正确的是
| A.三者对应的氧化物均为碱性氧化物 |
| B.三者的单质放置在空气中均只生成氧化物 |
| C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D.AlCl3、FeCl3、CuCl2均可用作净水剂 |

