题目内容
常温时,下列叙述正确的是??? (??? )
A.稀释pH=3的醋酸,溶液中所有离子的浓度均降低
B.一定浓度的CH3COOH和NaOH混合,溶液呈中性,则混合液中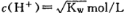
C.pH均为11的NaOH和Na2CO3溶液中,水的电离程度相同
D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多
【答案】
B
【解析】
试题分析: A中稀释pH=3的醋酸,溶液中氢氧根浓度增大,错误;B.一定浓度的CH3COOH和NaOH混合,溶液呈中性,氢离子和氢氧根浓度相等,根据水的离子积常数,可得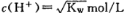 ,正确; C.pH均为11的NaOH和Na2CO3溶液中,前者是抑制了水的电离,后者是促进了水的电离,程度不相同,错误; D.由于醋酸是弱酸,pH与体积均相同的硫酸和醋酸,醋酸的物质的量多,消耗氢氧化钠的物质的量多,错误。
,正确; C.pH均为11的NaOH和Na2CO3溶液中,前者是抑制了水的电离,后者是促进了水的电离,程度不相同,错误; D.由于醋酸是弱酸,pH与体积均相同的硫酸和醋酸,醋酸的物质的量多,消耗氢氧化钠的物质的量多,错误。
考点:本题考查弱电解的电离平衡,盐类的水解。

练习册系列答案
相关题目