题目内容
主族元素A、B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍.A、B单质在常温下均为气体,它们在高温下以体积比2:1完全反应,生成物在常温下是液体.此液体与D单质能激烈反应生成A的单质.所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子.回答下列问题:
(1)写出元素符号A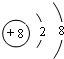
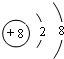 ;写出C元素在周期表中的位置第
;写出C元素在周期表中的位置第
(2)写出C在足量B中充分反应后生成物的电子式
 ,结构式
,结构式
(3)写出B、D在加热条件下形成化合物的电子式
 ,判断其中的化学键的类型
,判断其中的化学键的类型
 .
.
(4)写出一种有A、B、C、D组成的化合物的化学式
(1)写出元素符号A
H
H
,DNa
Na
.写出B阴离子结构示意图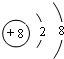
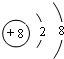
四
四
周期ⅣA
ⅣA
族;(2)写出C在足量B中充分反应后生成物的电子式


O=C=O
O=C=O
.(3)写出B、D在加热条件下形成化合物的电子式


离子键、共价键
离子键、共价键
.用电子式表示B、D在不加热条件下形成化合物的形成过程:

(4)写出一种有A、B、C、D组成的化合物的化学式
NaHCO3
NaHCO3
.分析:主族元素A、B、C、D的原子序数都小于18,C最外层电子数是次外层电子数的2倍,则C元素原子有2个电子层,最外层电子数为4,则C为碳元素;B与C在同一周期,C原子最外层电子数比B原子少2个,则B元素原子最外层电子数为6,则B为氧元素;A与D同主族,A、D原子的最外层电子数都是1,处于ⅠA族,A单质在常温下为气体,则A为氢元素,氢气与氢气在高温下以体积比2:1完全反应,生成物在常温下是液体为H2O,水与D单质能激烈反应生成A的单质,所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子,则D为Na元素,据此解答.
解答:解:主族元素A、B、C、D的原子序数都小于18,C最外层电子数是次外层电子数的2倍,则C元素原子有2个电子层,最外层电子数为4,则C为碳元素;B与C在同一周期,C原子最外层电子数比B原子少2个,则B元素原子最外层电子数为6,则B为氧元素;A与D同主族,A、D原子的最外层电子数都是1,处于ⅠA族,A单质在常温下为气体,则A为氢元素,氢气与氢气在高温下以体积比2:1完全反应,生成物在常温下是液体为H2O,水与D单质能激烈反应生成A的单质,所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子,则D为Na元素,
(1)由上述分析可知,A为H,D为Na;B阴离子为O2-,结构示意图为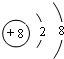 ;C为碳元素,在周期表中的位置第二周期ⅣA族,
;C为碳元素,在周期表中的位置第二周期ⅣA族,
故答案为:H;Na;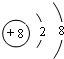 ;四;ⅣA;
;四;ⅣA;
(2)C在足量B中充分反应后生成物为CO2,其电子式为 ,结构式为O=C=O,
,结构式为O=C=O,
故答案为: ;O=C=O;
;O=C=O;
(3)B、D在加热条件下形成化合物为Na2O2,其电子式为 ,含有离子键、共价键,
,含有离子键、共价键,
B、D在不加热条件下形成化合物为Na2O,用电子式表示Na2O的形成过程: ,
,
故答案为: ;离子键、共价键;
;离子键、共价键; ;
;
(4)H、O、C、Na组成的化合物的化学式为NaHCO3等,故答案为:NaHCO3.
(1)由上述分析可知,A为H,D为Na;B阴离子为O2-,结构示意图为
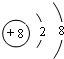 ;C为碳元素,在周期表中的位置第二周期ⅣA族,
;C为碳元素,在周期表中的位置第二周期ⅣA族,故答案为:H;Na;
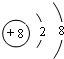 ;四;ⅣA;
;四;ⅣA;(2)C在足量B中充分反应后生成物为CO2,其电子式为
 ,结构式为O=C=O,
,结构式为O=C=O,故答案为:
 ;O=C=O;
;O=C=O;(3)B、D在加热条件下形成化合物为Na2O2,其电子式为
 ,含有离子键、共价键,
,含有离子键、共价键,B、D在不加热条件下形成化合物为Na2O,用电子式表示Na2O的形成过程:
 ,
,故答案为:
 ;离子键、共价键;
;离子键、共价键; ;
;(4)H、O、C、Na组成的化合物的化学式为NaHCO3等,故答案为:NaHCO3.
点评:本题考查结构性质位置关系、常用化学用语等,难度中等,注意掌握电子式等常用化学用语的书写.

练习册系列答案
相关题目




