题目内容
9.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )| A. | 0.5 mol 1,3-丁二烯分子中含有C=C双键数为 NA | |
| B. | 1 mol羟基(-OH)所含的电子总数为9NA | |
| C. | 14g乙烯、丙烯的混合气体中所含原子总数为3NA | |
| D. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为7/22.4NA |
分析 A、二烯烃中含2条碳碳双键;
B、羟基中含9个电子;
C、乙烯和丙烯的最简式均为CH2;
D、标况下庚烷为液态.
解答 解:A、二烯烃中含2条碳碳双键,故0.5mol丁二烯中含1mol碳碳双键即NA个,故A正确;
B、羟基中含9个电子,故1mol羟基中含9mol电子即9NA个,故B正确;
C、乙烯和丙烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量为n=$\frac{14g}{14g/mol}$=1mol,故含有3mol原子即3NA个,故C正确;
D、标况下庚烷为液态,故不能根据气体摩尔体积来计算其物质的量和燃烧产生的分子个数,故D错误.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
19.已知短周期元素的四种离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
| A. | 原子序数 d>c>b>a | |
| B. | 单质的还原性D<C<B<A | |
| C. | 离子半径 C3->D->B+>A2+ | |
| D. | A、B、C最高价氧化物对应水化物溶液(等物质的量浓度)的pH值C>B>A |

 ,
,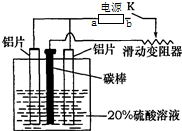 铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜.某化学研究小组在实验室中按下列步骤模拟该生产过程,装置如图.填写下列空白:
铝的阳极氧化,是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜.某化学研究小组在实验室中按下列步骤模拟该生产过程,装置如图.填写下列空白: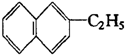 属于萘的同系物,则萘和萘的同系物分子组成通式为CnH2n-12 (n≥10).
属于萘的同系物,则萘和萘的同系物分子组成通式为CnH2n-12 (n≥10). ②丙的结构简式为
②丙的结构简式为 .
.