题目内容
2011年8月12日,网上传云南曲靖市越州镇有总量5000余吨的重毒化工废料铬渣由于非法丢放,毒水被直接排放南盘江中.
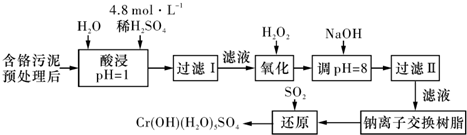
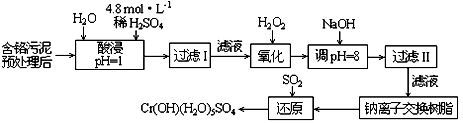
Ⅰ:某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
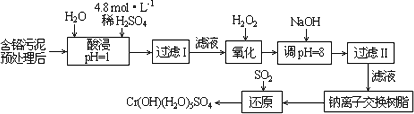
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
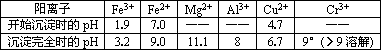
(1)实验室用18.4 mol·L-1的浓硫酸配制250 mL 4.8 mol·L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需________.
(2)酸浸时,为了提高浸取率可采取的措施是________(至少答一点).
(3)加入H2O2的作用是________.
调节溶液的pH=8是为了除去________离子.
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的的杂质离子是________.
(5)还原过程发生以下反应(请配平):
________Na2Cr2O7+________SO2+________=________Cr(OH)(H2O)5SO4+________Na2SO4;
Ⅱ:
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理.其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀.阳极的电极反应式为________.在阴极附近溶液pH升高的原因是(用电极反应方程式解释)________.解析:
|
Ⅰ:(1)250 mL容量瓶(1分)、胶头滴管(1分) (2)①升高反应温度,②搅拌,③过滤后再向滤渣中加入硫酸(多次浸取),④适当延长浸取时间(只要答出任意一点即可,可从反应温度、溶液的pH、搅拌速度、溶剂的配比等角度)(2分) (3)氧化+3价Cr使之转变成+6价Cr(或Cr2O72-),以便于与杂质离子分离(2分); Fe3+和Al3+(2分,各1分) (4)Ca2+、Mg2+(2分,各1分) (5)1,3,11H2O,2,1(2分), Ⅱ:Fe-2e-=Fe2+(2分),2H++2e-=H2↑(2分) |

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案已知:①重铬酸钾和铬酸酐都易溶于水,这是造成铬污染的主要原因,它们都是强氧化剂,铬酸酐溶于水呈酸性;
②+6价铬易被人体吸收,可致癌:+3价铬不易被人体吸收,毒性小.
③下表为一些金属氢氧化物沉淀的pH参照数据.
| 物质 | 开始沉淀 | 完全沉淀 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| Cr(OH)3 | 4.7 | a |
| Fe(OH)2 | 7.6 | 9.6 |
| Mg(OH)2 | 9.6 | 11.1 |
(1)将铬渣用稀硫酸浸取、过滤,在浸出液中加入适量的绿矾,加入绿矾的目的是 .
(2)再向浸出液中缓慢加入烧碱,至pH刚好达到4.7,过滤,所得沉淀的化学式是 ;常温下,Cr(OH)3的溶度积Ksp=10-32,要使Cr3+完全沉淀[c(Cr3+)降至10-5mol?L-1视为沉淀完全],溶液的pH应调于a= .
(3)向(2)中得到的滤液中加入硫酸,调节至呈强酸性,所得的溶液是含 溶质的溶液.