��Ŀ����
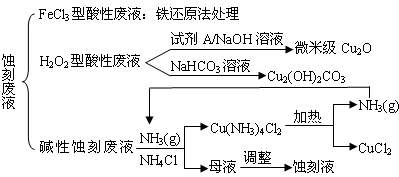
���꣬�ҹ����ӹ�ҵѸ�ٷ�չ������˴����ĵ�·���ʴ��Һ�IJ������ŷš���ʴҺ��Ҫ�����Ե�(HClH2O2)�����Ե�(NH3NH4Cl)�Լ���ͳ��(HClFeCl3)�����֣���ʴ��Һ�к��д�����Cu2������Һ�Ļ������ÿɼ���ͭ��Դ����ʧ�����ֿ�ʴ��Һ�ij�������������ͼ��

(1)FeCl3�����Է�Һ����ͭ��ʹ��ʴҺ��������������Ҫ���ӷ�Ӧ��Fe��Cu2��===Fe2����Cu,2Fe3����Fe===3Fe2��������___________________________________________________��
___________________________________________________________(���ӷ���ʽ��ʾ)��
(2)HClH2O2�Ϳ�ʴҺ��ʴCu�Ĺ����з����Ļ�ѧ��Ӧ�����ӷ���ʽ�ɱ�ʾΪ��________________________________________________________________________��
(3)H2O2�����Կ�ʴ��Һ����Cu2O�����У������Լ�A�����ѡ����________(�����)��
�����Ը��������Һ���ڹ���NaCl���ۼ�ȩ����������
(4)���Կ�ʴҺ�����ķ�Ӧ�ǣ�2Cu��O2��4NH4Cl��4NH3��H2O===2Cu(NH3)4Cl2��6H2O���������Կ�ʴ��Һ�����м���NH4Cl���岢ͨ��NH3(g)��Ŀ���ǣ�
________________________________________________________________________��
(1)Fe��2H��===Fe2����H2�� 2Fe2����Cl2===2Fe3����2Cl��
(2)Cu��2H����H2O2===Cu2����2H2O (3)��
(4)�ٽ���Һ�е�Cu(NH3)4Cl2���ɲ��ᾧ����
��������
���������(1)FeCl3�����Է�Һ�к�Fe3����Cu2����H���ȣ��������۽����ǻ�ԭ����ͨ��Cl2��Fe2��������
(2)��������H2O2����ԭ����Cu������������Cu2������ԭ������H2O�������ӷ���ʽ��֪��
(3)Ӧ�ü��뻹ԭ������ȩ����Ⱦ������ʹ�������Ǹ��á�
(4)����������Cu(NH3)4Cl2�ᾧ����������NH4Cl���岢ͨ��NH3(g)���Դٽ�Cu(NH3)4Cl2���ɲ���������ᾧ��
���㣺�������ʵķ�����ᴿ������ʽ����д��������ԭ��Ӧ���й�Ӧ�ú�ʵ�鷽�������
�����������Ǹ߿��еij������ͣ������ۺ���ǿ�������֪ʶ��࣬�ѶȽϴ�ѧ�����÷֡�����Ҫ��ѧ���������桢ϸ�µ����⣬��ϵ��ѧ����֪ʶ�ͼ��ܣ�����֪ʶ����ȡ�Ǩ�ơ����飬ȫ��ϸ�µ�˼�����ܵó���ȷ�Ľ��ۡ�