题目内容
(10分)某学习小组用右图装置进行了有关电化学的实验。在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅拌棒,可以上下搅动液体,装置如图。接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成。停止通电,取出电极,用搅拌棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。

根据上述实验回答:
(1)阳极上的电极反应式为_______________________。
(2)环状玻璃搅拌棒的作用是______________________。
(3)原上层液体是___________。
(4)原下层液体是___________。
(5)搅拌后两层液体颜色发生变化的原因是:___________________________________________。
(6)要检验上层液体中含有的金属离子,其方法是_ _____ ____,现象是___________________。
(1)2I--2e-==I2 (2)让两层液体充分混合,使I2转移到下层液体
(3)KI(或NaI等)水溶液 (4)CCl4(或CHCl3等)
(5)I2在CCl4中的溶解度大于在水中的溶解度,故大部分I2都转移到CCl4中
(6)焰色反应; 透过蓝色钴玻璃观察火焰呈紫色【其他合理答案同样给分:若(3)中答NaI水溶液,这里答火焰呈黄色】
【解析】
试题分析:阳极周围的液体呈现棕色,且颜色由浅变深,说明阳极发生氧化反应有碘生成,阳极反应式为 ;用下层液体萃取碘水中的碘单质,搅拌让两层液体充分混合,使I2转移到下层液体;(3)原溶液是中性液体,应该是强酸强碱盐的溶液,阳极有碘生成,所以原溶液含有
;用下层液体萃取碘水中的碘单质,搅拌让两层液体充分混合,使I2转移到下层液体;(3)原溶液是中性液体,应该是强酸强碱盐的溶液,阳极有碘生成,所以原溶液含有 ,原上层液体是KI(或NaI等)水溶液;原下层液体不溶于水,密度比水大,所以可能是CCl4(或CHCl3等);(5)搅拌后两层液体颜色发生变化的原因是:I2在CCl4中的溶解度大于在水中的溶解度,I2转移到下层液体;(6)碱金属的阳离子一般用焰色反应来检验,若透过蓝色钴玻璃观察火焰呈紫色,则含有K+;【其他若火焰呈黄色则含有Na+。
,原上层液体是KI(或NaI等)水溶液;原下层液体不溶于水,密度比水大,所以可能是CCl4(或CHCl3等);(5)搅拌后两层液体颜色发生变化的原因是:I2在CCl4中的溶解度大于在水中的溶解度,I2转移到下层液体;(6)碱金属的阳离子一般用焰色反应来检验,若透过蓝色钴玻璃观察火焰呈紫色,则含有K+;【其他若火焰呈黄色则含有Na+。
考点:本题考查电解原理、萃取、离子检验。

 Cu(OH)2?+Na2CO3
Cu(OH)2?+Na2CO3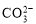 =CaCO3? , Ca(NO3)2+Na2CO3
=CaCO3? , Ca(NO3)2+Na2CO3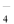 →MnO2 B.ClO3-→Cl-
→MnO2 B.ClO3-→Cl-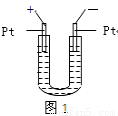
 2NH3(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
2NH3(g)的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是