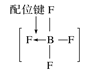
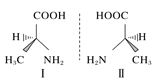
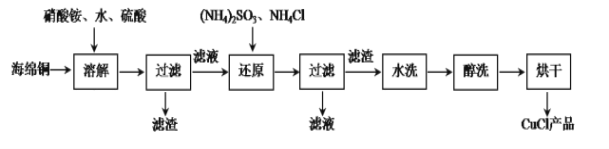
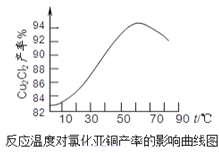
题目内容
【题目】能说明![]() 元素原子的得电子能力强于
元素原子的得电子能力强于![]() 元素原子的事实是( )
元素原子的事实是( )
A.![]() 元素位于
元素位于![]() 元素的上一个周期
元素的上一个周期
B.![]() 元素的含氧酸的酸性强于
元素的含氧酸的酸性强于![]() 元素的含氧酸
元素的含氧酸
C.分别加热![]() 、
、![]() 的简单氢化物
的简单氢化物![]() 、
、![]() 至500℃,只有
至500℃,只有![]() 发生分解
发生分解
D.![]() 元素与
元素与![]() 元素位于同一主族,在相同温度下二者的单质与铜反应分别生成
元素位于同一主族,在相同温度下二者的单质与铜反应分别生成![]() 和
和![]()
【答案】C
【解析】
元素原子的得电子能力是元素的非金属性的强弱的判据之一,即元素的非金属性越强,其原子得电子能力越强,据此分析作答。
A.同主族元素自上而下非金属性减弱,不是同主族则不一定,如非金属性:O>P,故A错误;
B.最高价含氧酸酸性越强,非金属性越强,不是最高价含氧酸不一定,如酸性:碳酸>HClO,故B错误;
C.加热H2X、HY至500℃,只有HY发生分解,说明HX更稳定,X元素的非金属性更强,故C正确;
D.单质与铜反应分别生成Cu2X和CuY,Y单质与铜反应得到高价态Cu,则Y的非金属性更强,故D错误;
故选:C。

练习册系列答案
相关题目