题目内容
(6分)(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个化学方程式并配平。
+  + + + H2O
+ + + H2O
(2)反应物中发生氧化反应的物质 ,被还原的元素是 。
(3)反应中1 mol氧化剂得到 mol电子。
(6分)(1)24FeSO4+30HNO3==8Fe(NO3)3+8Fe2(SO4)3+3N2O↑+15H2O (2分)
(2)FeSO4 N (各1分);(3)4 (2分)。
【解析】
试题分析:(1)根据氧化性:氧化剂>氧化产物,硝酸是强氧化剂,能够氧化许多有还原性的物质。该反应的方程式是:24FeSO4+30HNO3==8Fe(NO3)3+8Fe2(SO4)3+3N2O↑+15H2O;(2)在反应物中发生氧化反应的物质还原剂FeSO4;氧化剂是HNO3 ,其中被还原的元素是N元素;(3)由于反应前N的化合价是+5价。,反应后N元素的化合价是+1价,所以在反应中1 mol氧化剂得到4mol的电子。
考点:考查氧化还原反应的方程式的配平、发生氧化、还原的元素及电子转移的知识。

练习册系列答案
相关题目
X 、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是
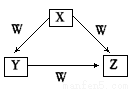
| X | Y | Z | W |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |