题目内容
以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下
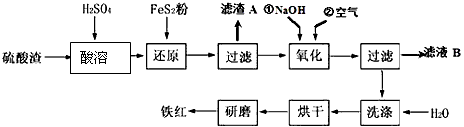
(1)酸溶过程中Fe2O3与稀硫酸反应的化学方程式为___________________________; “滤渣A”主要成份的化学式为___________。
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2 + 14Fe3+ +____H2O== 15Fe2+ +_____SO42- +___________。
(3)氧化过程中,O2、NaOH与Fe2+反应的离子方程式为____________________________。
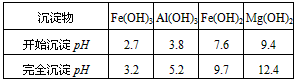
(4)为了确保铁红的质量,氧化过程需要调节溶液的pH的范围是___________(几种离子沉淀的pH见下表);滤液B可以回收的物质有(写化学式)___________。
(2)还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2 + 14Fe3+ +____H2O== 15Fe2+ +_____SO42- +___________。
(3)氧化过程中,O2、NaOH与Fe2+反应的离子方程式为____________________________。
(4)为了确保铁红的质量,氧化过程需要调节溶液的pH的范围是___________(几种离子沉淀的pH见下表);滤液B可以回收的物质有(写化学式)___________。
(1)Fe2O3+3H2SO4==Fe2(SO4)3+3H2O;SiO2
(2)8;2;16H+
(3)4Fe2++O2+2H2O+8OH-==4Fe(OH)3↓ (Fe2++2OH-==Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3)
(4)3.2~3.8(或二者之间的数据值);Na2SO4、Al2(SO4)3、MgSO4
(2)8;2;16H+
(3)4Fe2++O2+2H2O+8OH-==4Fe(OH)3↓ (Fe2++2OH-==Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3)
(4)3.2~3.8(或二者之间的数据值);Na2SO4、Al2(SO4)3、MgSO4

练习册系列答案
 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:

(1)硫酸渣的成分中属于两性氧化物的是 , 写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式: ;
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是_________;(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
|
沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Fe(OH)2 |
Mg(OH)2 |
|
开始沉淀 |
2.7 |
3.8 |
7.5 |
9.4 |
|
完全沉淀 |
3.2 |
5.2 |
9.7 |
12.4 |
(3)滤渣A的主要成分为 ,滤液B可以回收的物质有______________________;
(4)简述洗涤过程的实验操作 ;
(5)已知硫酸渣质量为w kg,假设铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来硫酸渣中铁元素质量分数为 (用最简分数表达式表示)。
(已知相对原子质量:O 16 S 32 Fe 56 )
 (2011?镇江一模)以黄铁矿为原料制硫酸产生的废渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等.现以此废渣制备铁红(Fe2O3)的过程如下.此浓度时,部分阳离子以氢氧化物形式沉淀时溶液的pH由见表.
(2011?镇江一模)以黄铁矿为原料制硫酸产生的废渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等.现以此废渣制备铁红(Fe2O3)的过程如下.此浓度时,部分阳离子以氢氧化物形式沉淀时溶液的pH由见表.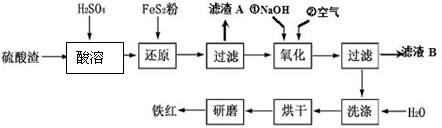
 和
和
