题目内容
15.下列电解质的电离方程式错误的是( )| A. | HCl═H++C1- | B. | NaOH═Na++O2-+H+ | ||
| C. | BaCl2═Ba2++2C1- | D. | CuSO4═Cu2++SO42- |
分析 A.HCl是强电解质水溶液中完全电离;
B.NaOH是强电解质水溶液中完全电离出钠离子和氢氧根离子;
C.BaCl2是强电解质水溶液中完全电离;
D.硫酸铜是强电解质,在溶液中完全电离出硫酸根离子和铜离子.
解答 解:A.HCl是强电解质水溶液中完全电离,其电离方程式为:HCl═H++C1-,故A正确;
B.NaOH是强电解质水溶液中完全电离出钠离子和氢氧根离子,其电离方程式为:NaOH═Na++OH-,故B错误;
C.BaCl2是强电解质水溶液中完全电离,其电离方程式为:BaCl2═Ba2++2C1-;故C正确;
D.硫酸铜是强电解质,在溶液中完全电离出硫酸根离子和铜离子,其电离方程式为:CuSO4═Cu2++SO42-,故D正确.
故选B.
点评 本题考查电离方程式,注意强电解质在溶液中能完全电离,弱电解质部分电离,离子团在电离方程式中不能拆开,强酸的酸式根离子要拆开,弱酸的酸式根离子不能拆开,碳酸氢钠电离为该题易错点,题目难度不大.

练习册系列答案
相关题目
5.下列物质在光照时不反应的是( )
| A. | 氢气和氯气的混合气体 | B. | 硝酸 | ||
| C. | 氢气和氧气的混合气体 | D. | 氯水 |
6.下列物质使用(括号内为用途)不正确的是( )
| A. | 碳酸钠(发酵粉) | B. | Ca(ClO)2(消毒剂) | C. | Al2O3(耐火材料) | D. | 过氧化钠(供氧剂) |
3.下列关于著名科学家的国籍、名字和研究成果的对应关系中,正确的是( )
| A. | 英国道尔顿----提出元素概念 | |
| B. | 法国拉瓦锡----提出原子学说 | |
| C. | 汤姆生---发现电子 | |
| D. | 英国波义耳----建立燃烧现象的氧化学说 |
20.下列反应的离子方程式书写正确的是( )
| A. | 铁粉溶于稀盐酸:2Fe+6H+═2Fe3++3H2 | |
| B. | 碳酸钙溶于稀盐酸中:CO32-+2H+═CO2+H2O | |
| C. | 氧化铜溶于醋酸:CuO+2CH3COOH═Cu2++2CH3COO-+H2O | |
| D. | 硫酸铜与氢氧化钡溶液混合:Ba2++SO42-═BaSO4 |
4.标准状况下,下列物质所占体积最大的是( )
| A. | 6.72 LN2 | B. | 6.02×1023个 CO2 | C. | 6 g H2 | D. | 196 g H2SO4 |

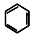 +CH2=CH2$\stackrel{H_{2}SO_{4}}{→}$
+CH2=CH2$\stackrel{H_{2}SO_{4}}{→}$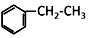
 .
. .
.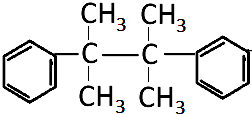 .
.