题目内容
7.下列电离方程式中,不正确的是( )| A. | KCl═K++Cl- | B. | NH3•H2O?NH4++OH- | ||
| C. | CH3COOH═CH3COO-+H+ | D. | HCl═H++Cl- |
分析 分清电解质的强弱,强电解质在水溶液里完全电离生成阴阳离子,电离方程式写“=”,弱电解质在水溶液里部分电离,电离方程式写“?”,书写时要遵循原子守恒、电荷守恒,据此分析解答.
解答 解:A.KCl为强电解质,完全电离,电离方程式为KCl=K++Cl-,故A正确;
B.NH3•H2O为弱电解质,部分电离,电离方程式为NH3•H2O?NH4++OH-,故B正确;
C.CH3COOH为弱电解质,部分电离,电离方程式为CH3COOH?CH3COO-+H+,故C错误;
D.HCl为强电解质,完全电离,电离方程式为HCl═H++Cl-,故D正确;
故选C.
点评 本题主要考查学生电离方程式的书写知识,明确电解质的强弱是解题关键,注意原子团不能拆,题目难度不大.

练习册系列答案
相关题目
12. 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A. | 将1.0 mol氮气、3.0 mol氢气,置于1 L密闭容器中发生反应,放出的热量为 92.4 kJ | |
| B. | 平衡状态由A变到B时,平衡常数K (A)<K (B) | |
| C. | 上述反应在达到平衡后,增大压强,H2的转化率提高 | |
| D. | 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速度减小 |
18.下列反应最终无沉淀产生的是( )
①过量的CO2通入Na2SiO3溶液中 ②向氢氧化铝溶液中滴加氢氧化钠溶液至过量
③少量的SO2通入BaCl2溶液中 ④向MgCl2溶液中滴加NaOH溶液至过量.
①过量的CO2通入Na2SiO3溶液中 ②向氢氧化铝溶液中滴加氢氧化钠溶液至过量
③少量的SO2通入BaCl2溶液中 ④向MgCl2溶液中滴加NaOH溶液至过量.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ①④ |
15.Ⅰ.碱性锌锰干电池是最常见的化学电源之一,已知其电池总反应:
Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极发生反应的物质为Zn+2OHˉ-2eˉ=Zn(OH)2;发生在正极的电极反应为MnO2+H2O+e-=MnO(OH)+OH-.
Ⅱ.回收的废旧锌锰干电池经过处理后得到锰粉(含MnO2、MnOOH、Fe和炭黑等),由锰粉制取MnO2的步骤如图所示:
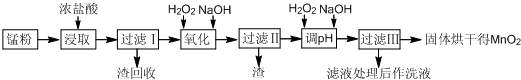
根据如图所示步骤并参考表格数据回答问题:
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等.加热的作用是加快反应速率.
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入适量H2O2溶液,其作用是将Fe2+转化为Fe3+.
(3)将过滤I所得滤液经H2O2氧化后,再加入NaOH溶液调节pH的范围是:3.7<pH<8.3,其目的是使Fe3+完全沉淀,并防止Mn2+转化为Mn(OH)2沉淀.
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为Mn2++H2O2+2OH-=MnO2↓+2H2O.
(5)实验室进行过滤操作时,需要用到的玻璃仪器有漏斗、烧杯、玻璃棒.
Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极发生反应的物质为Zn+2OHˉ-2eˉ=Zn(OH)2;发生在正极的电极反应为MnO2+H2O+e-=MnO(OH)+OH-.
Ⅱ.回收的废旧锌锰干电池经过处理后得到锰粉(含MnO2、MnOOH、Fe和炭黑等),由锰粉制取MnO2的步骤如图所示:

| 开始沉淀 | 沉淀完全 | |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
(1)在加热条件下用浓盐酸浸取锰粉,所得溶液中含有Mn2+、Fe2+等.加热的作用是加快反应速率.
(2)锰粉经浓盐酸浸取,过滤I除去不溶杂质后,向滤液中加入适量H2O2溶液,其作用是将Fe2+转化为Fe3+.
(3)将过滤I所得滤液经H2O2氧化后,再加入NaOH溶液调节pH的范围是:3.7<pH<8.3,其目的是使Fe3+完全沉淀,并防止Mn2+转化为Mn(OH)2沉淀.
(4)过滤Ⅱ所得滤液加入足量H2O2溶液并加入NaOH溶液调节pH约为9,使Mn2+氧化得到MnO2,反应的离子方程式为Mn2++H2O2+2OH-=MnO2↓+2H2O.
(5)实验室进行过滤操作时,需要用到的玻璃仪器有漏斗、烧杯、玻璃棒.
2.现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(2)某同学根据上述信息,所画的B电子排布图如图 ,违背了泡利原理.
,违背了泡利原理.
(3)F位于周期表中第四周期、ⅦB族、d区,其基态原子有25种运动状态.
(4)CD3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形,检验E元素的方法是焰色反应.
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
(2)某同学根据上述信息,所画的B电子排布图如图
 ,违背了泡利原理.
,违背了泡利原理.(3)F位于周期表中第四周期、ⅦB族、d区,其基态原子有25种运动状态.
(4)CD3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形,检验E元素的方法是焰色反应.
12.可逆反应mA(g)+nB(g)?pC(g)+qD(g)的v-t图象如图,若其它条件不变,只是在反应前加入合适的催化剂,其v-t图象如图:则①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大,以上说法中不正确的是(  )
)
 )
)| A. | ②④⑤⑦ | B. | ①④⑥⑧ | C. | ②③⑤⑧ | D. | ①③⑥⑧ |
19.CoCl2•xH2O在加热时会逐步失水,并呈现不同的颜色,实验室里可以制成变色硅胶,用以干燥并验证水份.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种新工艺流程如图:

已知:
①钴与盐酸反应的化学方程式为:Co+2HCl═CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)写出加入过氧化氢时溶液中发生的离子反应方程式:2Fe2++H2O2+2H+=2Fe3++2H2O
(2)加入碳酸钠调节pH至a,a的范围是5.2~7.6;
(3)最合适的试剂X是盐酸
(4)操作I包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和减压过滤.
(5)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.

已知:
①钴与盐酸反应的化学方程式为:Co+2HCl═CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Co(OH)3 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.2 | 5.2 |
(1)写出加入过氧化氢时溶液中发生的离子反应方程式:2Fe2++H2O2+2H+=2Fe3++2H2O
(2)加入碳酸钠调节pH至a,a的范围是5.2~7.6;
(3)最合适的试剂X是盐酸
(4)操作I包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和减压过滤.
(5)制得的CoCl2•6H2O需减压烘干的原因是降低烘干温度,防止产品分解.
16.标准状况下质量为4g H2的体积约为( )
| A. | 11.2 L | B. | 22.4 L | C. | 33.6 L | D. | 44.8 L |
17.在容积一定的密闭窗口中,反应A?B(g)+C(s)达平衡,若继续升高温度,容器内气体的密度增大,下列判断正确的是( )
| A. | 压强对该反应的平衡移动没有影响 | |
| B. | 在平衡体系中加入C,混合气体平均分子量增大 | |
| C. | 若正反应为吸热反应,则A为非气态 | |
| D. | 若正反应为放热反应,则A为非气态 |