题目内容
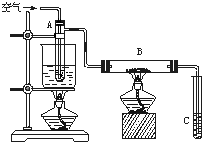 某课外活动小组用如图所示进行乙醇的催化氧化实验探究,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体),试管C中放的是蒸馏水.请回答下列问题:
某课外活动小组用如图所示进行乙醇的催化氧化实验探究,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体),试管C中放的是蒸馏水.请回答下列问题:(1)向试管A中鼓入空气的目的是
(2)玻璃管B中可观察到的现象是
相关化学方程式是
(3)在实验过程中试管C导管口有气泡冒出,从液面逸出的气体的主要成分是
(4)烧杯中水的作用是
分析:(1)乙醇和氧气在铜作催化剂条件下加热发生氧化还原反应生成乙醛,乙醇在加热条件下也可与氧化铜反应生成乙醛,则A中鼓入空气可提供氧气和乙醇的混合气体;
(2)玻璃管B中乙醇和氧化铜发生反应,氧化铜为黑色,生成铜为红色,根据反应原理书写方程式.据此解答;
(3)根据氧气和乙醇反应结合气体的溶解度分析从液面逸出的气体的主要成分是氮气,试管C的溶液含有醛基,
与新制的Cu(OH)2悬浊液反应有氧化亚铜生成;
(4)水浴加热的温度是使反应容器内试剂受热温度均匀,便于控制温度;
(2)玻璃管B中乙醇和氧化铜发生反应,氧化铜为黑色,生成铜为红色,根据反应原理书写方程式.据此解答;
(3)根据氧气和乙醇反应结合气体的溶解度分析从液面逸出的气体的主要成分是氮气,试管C的溶液含有醛基,
与新制的Cu(OH)2悬浊液反应有氧化亚铜生成;
(4)水浴加热的温度是使反应容器内试剂受热温度均匀,便于控制温度;
解答:解:(1)A中通入空气的目的是提供氧化乙醇的氧化剂氧气并形成乙醇和空气的混合气体,
故答案为:使空气通过乙醇,形成乙醇和空气的混合气体;
(2)乙醇和氧化铜在加热条件下发生氧化还原反应,-CH2OH结构被氧化为-CHO结构,生成乙醛,反应的方程式为CuO+C2H5OH
CH3CHO+H2O+Cu,可观察到黑色固体变红,
故答案为:黑色固体变红; CuO+C2H5OH
CH3CHO+H2O+Cu;
(3)氧气和乙醇发生氧化还原反应,最终气体含有乙醇、乙醛和氮气,由于乙醇、乙醛易溶于水,则最终气体为氮气,试管C的溶液主要成分为乙醛,乙醛和新制的Cu(OH)2悬浊液反应生成乙酸和氧化亚铜和水,所以观察到有砖红的沉淀产生,
故答案为:N2;有红色沉淀产生;
(4)水的沸点是100℃,用水浴加热,使反应容器内试剂受热温度均匀,便于控制温度,
故答案为:使试管受热均匀,便于控制温度.
故答案为:使空气通过乙醇,形成乙醇和空气的混合气体;
(2)乙醇和氧化铜在加热条件下发生氧化还原反应,-CH2OH结构被氧化为-CHO结构,生成乙醛,反应的方程式为CuO+C2H5OH
| △ |
故答案为:黑色固体变红; CuO+C2H5OH
| △ |
(3)氧气和乙醇发生氧化还原反应,最终气体含有乙醇、乙醛和氮气,由于乙醇、乙醛易溶于水,则最终气体为氮气,试管C的溶液主要成分为乙醛,乙醛和新制的Cu(OH)2悬浊液反应生成乙酸和氧化亚铜和水,所以观察到有砖红的沉淀产生,
故答案为:N2;有红色沉淀产生;
(4)水的沸点是100℃,用水浴加热,使反应容器内试剂受热温度均匀,便于控制温度,
故答案为:使试管受热均匀,便于控制温度.
点评:本题以乙醇的催化氧化为载体考查学生的分析能力和实验设计能力,为高频考点,注意把握乙醇的性质以及实验的可行性的评价,题目难度中等.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目

 某课外活动小组用如图所示装置进行实验(电解液足量).下列说法正确的是( )
某课外活动小组用如图所示装置进行实验(电解液足量).下列说法正确的是( )

