题目内容
 某课外活动小组用如图所示装置进行实验(电解液足量).下列说法正确的是( )
某课外活动小组用如图所示装置进行实验(电解液足量).下列说法正确的是( )分析:图一中若开始实验时开关K与a连接,则形成原电池,图一中若开始实验时开关K与b连接,则形成电解池,铁棒作阴极,
图二中若开始实验时开关K与a连接,则形成原电池,图二中若开始实验时开关K与b连接,相当于电镀装置,以此解答.
图二中若开始实验时开关K与a连接,则形成原电池,图二中若开始实验时开关K与b连接,相当于电镀装置,以此解答.
解答:解:A.图一中若开始实验时开关K与a连接,则形成原电池,B极的电极反应式应为Fe-2e-═Fe2+,故A错误;
B.图一中若开始实验时开关K与b连接,则形成电解池,铁棒作阴极,电解的总反应式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑,根据质量守恒可知一段时间后向电解液中通入适量的HCl可使电解液恢复到电解前的浓度,故B错误;
C.图二中若开始实验时开关K与a连接,则形成原电池,电池的总反应式为Fe+2AgNO3═Fe(NO3)2+2Ag,电解液的浓度减小,故C错误;
D.图二中若开始实验时开关K与b连接,相当于电镀装置,溶液浓度不变,故D正确.
故选:D.
B.图一中若开始实验时开关K与b连接,则形成电解池,铁棒作阴极,电解的总反应式为2NaCl+2H2O
| ||
C.图二中若开始实验时开关K与a连接,则形成原电池,电池的总反应式为Fe+2AgNO3═Fe(NO3)2+2Ag,电解液的浓度减小,故C错误;
D.图二中若开始实验时开关K与b连接,相当于电镀装置,溶液浓度不变,故D正确.
故选:D.
点评:本题综合考查原电池和电解池知识,为高考常见题型,侧重于学生的分析能力和基本理论的综合运用,难度不大,注意把握电化学原理和电极方程式的书写,难度不大.

练习册系列答案
相关题目

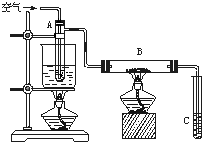 某课外活动小组用如图所示进行乙醇的催化氧化实验探究,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体),试管C中放的是蒸馏水.请回答下列问题:
某课外活动小组用如图所示进行乙醇的催化氧化实验探究,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体),试管C中放的是蒸馏水.请回答下列问题:

