题目内容
25℃时,某浓度的氯化铵溶液的pH=4,下列叙述中正确的是
- A.溶液中的 c(OH-)=1×10 -10mol·L-1
- B.溶液中的c(NH4+)>c(Cl-)>c(H+)>c(OH-)
- C.溶液中的c(H+)+ c(NH4+)= c(Cl-)+ c(OH-)
- D.溶液中的c(NH3·H2O)= c(NH4+)
AC
正确答案:AC
A、正确,c(OH-)=Kw/1×10 -4mol·L-1=1×10 -10mol·L-1
B、不正确,NH4+要水解,c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C、正确,电荷守恒;
D、不正确,物料守恒c(NH3·H2O)+ c(NH4+)= c(Cl-)
正确答案:AC
A、正确,c(OH-)=Kw/1×10 -4mol·L-1=1×10 -10mol·L-1
B、不正确,NH4+要水解,c(Cl-)>c(NH4+)>c(H+)>c(OH-)
C、正确,电荷守恒;
D、不正确,物料守恒c(NH3·H2O)+ c(NH4+)= c(Cl-)

练习册系列答案
相关题目
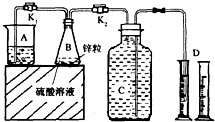 某化学兴趣小组用如图装置进行“市售锌粒和硫酸反应制取氢气的条件选择”的探究:当B中的化学反应趋于平稳后,每间隔一分钟收集一次氢气.不同条件下,每分钟收集到氢气的体积如下表:
某化学兴趣小组用如图装置进行“市售锌粒和硫酸反应制取氢气的条件选择”的探究:当B中的化学反应趋于平稳后,每间隔一分钟收集一次氢气.不同条件下,每分钟收集到氢气的体积如下表:| 实验序号 | 硫酸浓度 | 饱和硫酸铜溶液体积/mL | 反应达到平稳的时间/min | 第1分钟收集氢气体积/mL | 第2分钟收集氢气体积/mL | 第3分钟收集氢气体积/mL | … |
| 1 | 20% | 0 | 5.4 | 6.1 | 11.9 | 13.7 | … |
| 2 | 20% | 0.5 | 2.5 | 23.9 | 32.1 | 33.5 | … |
| 3 | 30% | 0.5 | 1.1 | 60.7 | 89.9 | 90.1 | … |
| 4 | a% | 3.0 | 0.8 | 55.7 | 66.0 | 61.4 | … |
(1)关闭K2、打开K1,观察到
(2)实验l、2是对比探究实验,分析上表,说明该对比探究实验的目的是
(3)细口瓶C的容积为V(mL),为了使加入的锌(质量bg)不浪费,在C中还留有
| 2 |
| 5 |
(4)实验4是研究饱和硫酸铜溶液的体积对实验的影响,a值应为
A. 20 B.30 C.27 D. 40
(5)分析上表,市售锌粒和硫酸反应制取氢气的条件应该选择实验
(6)从实验后的废液中回收皓矾(ZnSO4?7H2O)所需的实验操作步骤是
(7)查资料得知:Cu++Cl-═CuCl↓.
湿法冶锌工艺中,硫酸锌溶液中常含有少量的氯离子,往其中加硫酸铜溶液和金属锌,可除去氯离子,其离子反应方程式是
 2Z
2Z