题目内容
1.关于反应速率的说法中,正确的是( )| A. | 反应速率用于衡量化学反应进行的快慢 | |
| B. | 决定反应速率的本质因素是反应温度 | |
| C. | 可逆反应达到化学平衡时,正逆反应速率都为0 | |
| D. | 增加反应物物质的量,能增大反应速率 |
分析 A.反应速率越大,反应越快;
B.影响化学反应速率的主要因素为物质的性质;
C.化学反应达到平衡状态时,正逆反应速率相等,但不为0;
D.增加反应物物质的量,如浓度不变,则反应速率不变.
解答 解:A.反应速率越大,反应越快,所以反应速率用于衡量化学反应进行的快慢,故A正确;
B.影响化学反应速率的主要因素为物质的性质,其次有浓度、温度、催化剂以及压强等,故B错误;
C.化学反应达到平衡状态时,正逆反应速率相等,但变为0,反应继续进行,故C错误;
D.如增加固体的量,则浓度不变,反应速率不变,故D错误.
故选A.
点评 本题考查化学反应速率的因素,题目难度不大,注意影响化学反应速率的主要原因是物质的性质,为内因,温度、浓度、压强、催化剂等为外因.

练习册系列答案
相关题目
6.下列化学反应中,HCl部分被氧化的是( )
| A. | NaOH+HCl=NaCl+H2O | B. | 4HCl+MnO2=Cl2↑+MnCl2+2H2O | ||
| C. | HCl+AgNO3=AgCl↓+HNO3 | D. | CaO+2HCl=CaCl2+H2O |
9.下列除去杂质的方法中正确的是( )
①除去乙烷中少量的乙烯:通入适量H2,加催化剂反应
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液、干燥、蒸馏
③除去硝基苯中少量的NO2:滴入适量的NaOH溶液后,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去蛋白质中少量离子:用半透膜,渗析.
①除去乙烷中少量的乙烯:通入适量H2,加催化剂反应
②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液、干燥、蒸馏
③除去硝基苯中少量的NO2:滴入适量的NaOH溶液后,过滤
④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
⑤除去蛋白质中少量离子:用半透膜,渗析.
| A. | ①②④ | B. | ②③④ | C. | ②④⑤ | D. | ③④⑤ |
16.下列有关乙醇的物理性质的应用中不正确的是( )
| A. | 乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去 | |
| B. | 乙醇能溶解很多有机物和无机物,可用乙醇提取中药中的有效成分 | |
| C. | 乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒 | |
| D. | 乙醇容易挥发,所以才有“酒香不怕巷子深”的俗语 |
6.如表对应关系不正确的是( )
| 序号 | 俗称 | 主要成分 | 主要作用或用途 |
| A | 漂白粉 | Ca(ClO)2和CaCl2 | 可做漂白剂或环境消毒剂 |
| B | 硅胶 | H2SiO3 | 可做实验室或袋装食品、瓶装药品的干燥剂 |
| C | 石英 | SiO2 | 可做饰品、光纤材料以及半导体材料等 |
| D | 纯碱 | Na2CO3 | 可用于造纸、制玻璃等 |
| A. | A | B. | B | C. | C | D. | D |
13.下列对有机物结构或性质的描述,不正确的是( )
| A. | 苯分子中的6个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的独特的键 | |
| B. | 将溴水加入苯中,震荡,溴水的颜色变浅,这是由于发生了加成反应 | |
| C. | 乙烷和丙烯的混合物共1 mol,完全燃烧生成3 mol H2O | |
| D. | 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 |
10.1mol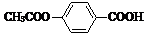 在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
 在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )| A. | 2mol | B. | 3 mol | C. | 4 mol | D. | 5 mol |
11.下列制备和收集气体的实验装置合理的是( )
| A. | 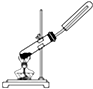 用氯化铵和氢氧化钠固体制NH3 | B. | 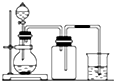 用铜片和稀硝酸制NO | ||
| C. | 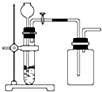 用锌粒和稀硫酸制H2 | D. | 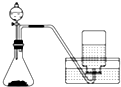 用H2O2和MnO2制O2 |

 ;
;