题目内容
一定体积的N2、O2、CO2混合气体通过足量的Na2O2后,同温同压下体积变为原来的0.75倍,原混合气体中N2、O2、CO2物质的量之比可能为( )
A.1∶2∶1 B.4∶3∶5 C.1∶1∶2 D.6∶7∶14
【答案】
C
【解析】设原混合气体中N2、O2、CO2物质的量分别是abc,通过过氧化钠时CO2反应,方程式为2Na2O2+2CO2=2Na2CO3+O2,所以反应后的气体是氮气和氧气,则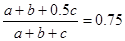 ,解得a+b=c,所以选项C正确,其余都是错误的,答案选C。
,解得a+b=c,所以选项C正确,其余都是错误的,答案选C。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一定体积的N2、O2、CO2混合气体通过足量的Na2O2后,同温同压下体积变为原来的0.75倍,
原混合气体中N2、O2、CO2物质的量之比可能为( )
| A.1∶2∶1 | B.4∶3∶5 | C.1∶1∶2 | D.6∶7∶14 |