题目内容
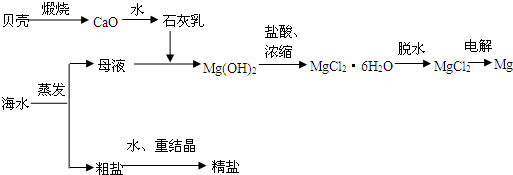
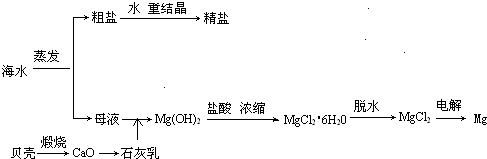
海水的综合利用可以制备金属镁,其流程如下图所示:
(1)若在空气中加热MgCl2·6H2O,生成的是 Mg(OH)Cl或MgO,写出相应反应的化学方程式________。
用电解法制取金属镁时,需要无水氯化镁。在干燥的HCl气流中加热MgCl26H2O时,能得到无水MgCl2,其原因是________。
(2)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。________。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:________;
过滤时:________;
蒸发时:________。
答案:
解析:
解析:
| (1)MgCl2·6H2O (2)加入MgCl2溶液,充分搅拌,过滤,沉淀用水洗涤 (3)搅拌,加速溶解 使待滤液体沿玻璃棒流入漏斗,防止外洒搅拌,防止因局部过热液滴或晶体飞溅
|

练习册系列答案
相关题目