ЬтФПФкШн
ЁОЬтФПЁПЕЊЕФбѕЛЏЮяЪЧдьГЩДѓЦјЮлШОЕФжївЊЮяжЪЁЃбаОПЕЊбѕЛЏЮяЕФЗДгІЛњРэЃЌЖдгкЯћГ§ЛЗОГЮлШОгаживЊвтвхЁЃЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉвбжЊ2NO(g) +O2(g)![]() -2NO2(g) ЁїHЕФЗДгІРњГЬЗжСНВНЃК
-2NO2(g) ЁїHЕФЗДгІРњГЬЗжСНВНЃК
Ђй2NO( g )![]() N2O2 (g)( Пь ) ЁїH1<0ЃЌv1е§=k1е§c2(NO)ЃЌv1Фц=k1Фцc2(N2O2)
N2O2 (g)( Пь ) ЁїH1<0ЃЌv1е§=k1е§c2(NO)ЃЌv1Фц=k1Фцc2(N2O2)
ЂкN2O2 (g)+ O2 (g) ![]() 2NO2(g)(Т§) ЁїH2<0ЃЌv2е§=k2е§c2(N2O2)c(O2)ЃЌv2Фц=k2Фцc2(NO2)
2NO2(g)(Т§) ЁїH2<0ЃЌv2е§=k2е§c2(N2O2)c(O2)ЃЌv2Фц=k2Фцc2(NO2)
БШНЯЗДгІЂйЕФЛюЛЏФмE1гыЗДгІЂкЕФЛюЛЏФмE2ЕФДѓаЁ: E1__ E2 (ЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБ) ЦфХаЖЯРэгЩЪЧ__________ЃЛ2NO(g) +O2(g)![]() 2NO2(g) ЕФЦНКтГЃЪ§KгыЩЯЪіЗДгІЫйТЪГЃЪ§k1е§ЁЂk1ФцЁЂk2е§ЁЂ k2ФцЕФЙиЯЕЪНЮЊ_______ЃЛвбжЊЗДгІЫйТЪГЃЪ§kЫцЮТЖШЩ§ИпЖјдіДѓЃЌШєЩ§ИпЮТЖШКѓk2е§ЁЂ k2ФцЗжБ№діДѓaБЖКЭbБЖЃЌдђa____b (ЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБ)ЃЛвЛЖЈЬѕМўЯТЃЌ2NO (g)+O2(g)
2NO2(g) ЕФЦНКтГЃЪ§KгыЩЯЪіЗДгІЫйТЪГЃЪ§k1е§ЁЂk1ФцЁЂk2е§ЁЂ k2ФцЕФЙиЯЕЪНЮЊ_______ЃЛвбжЊЗДгІЫйТЪГЃЪ§kЫцЮТЖШЩ§ИпЖјдіДѓЃЌШєЩ§ИпЮТЖШКѓk2е§ЁЂ k2ФцЗжБ№діДѓaБЖКЭbБЖЃЌдђa____b (ЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБ)ЃЛвЛЖЈЬѕМўЯТЃЌ2NO (g)+O2(g) ![]() 2NO2 (g)ДяЦНКтКѓЃЌЩ§ИпЕНФГЮТЖШЃЌдйДяЦНКтКѓv2е§НЯдЦНКтМѕаЁЃЌИљОнЩЯЪіЫйТЪЗНГЬЗжЮіЃЌКЯРэЕФНтЪЭЪЧ_________________ЁЃ
2NO2 (g)ДяЦНКтКѓЃЌЩ§ИпЕНФГЮТЖШЃЌдйДяЦНКтКѓv2е§НЯдЦНКтМѕаЁЃЌИљОнЩЯЪіЫйТЪЗНГЬЗжЮіЃЌКЯРэЕФНтЪЭЪЧ_________________ЁЃ
ЃЈ2ЃЉЂйвдввЯЉ(C2H4)зїЮЊЛЙдМСЭбЯѕ(NO)ЃЌЦфЭбЯѕЛњРэШчзѓЯТЭМЫљЪОЃЌШєЗДгІжаn(NO): n(O2) =2 ЃК1ЃЌдђзмЗДгІЕФЛЏбЇЗНГЬЪНЮЊ_______________ЃЛЭбЯѕТЪгыЮТЖШЁЂИКдиТЪ(ЗжзгЩИжаДпЛЏМСЕФжЪСПЗжЪ§) ЕФЙиЯЕШчгвЯТЭМЃЌЮЊДяЕНзюМбЭбЯѕаЇЙћЃЌгІВЩгУЕФЬѕМўЪЧ________________ЁЃ
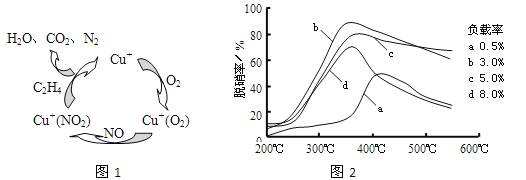
ЂкгУNOПЩжБНгДпЛЏNOЗжНтЩњГЩN2ЁЂO2ЃЌНЋЦфЗДгІЛњРэВЙГфЭъећ(VoДњБэбѕПебЈ)ЃК
2Ni2++2Vo+2NOЁњ2Ni3++2O-+N2 2O-ЁњO2-+1/2O2+Vo ______________
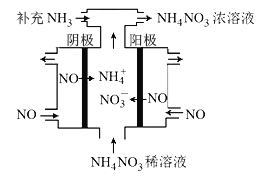
ЃЈ3ЃЉЕчНтNOПЩжЦБИNH4NO3ЃЌЦфЙЄзїдРэШчЭМЫљЪОЃЌвѕМЋЕФЕчМЋЗДгІЪНЮЊ______________ЁЃ
ЁОД№АИЁП ЃМ ЛюЛЏФмдНДѓЃЌвЛАуЗжзгГЩЮЊЛюЛЏЗжзгдНФбЃЌЗДгІЫйТЪдНТ§ ![]() ЃМ ЮТЖШЩ§ИпЃЌЗДгІЂйЁЂЂкЕФЦНКтОљФцвЦЃЌгЩгкЗДгІЂйЕФЫйТЪДѓЃЌЕМжТc(N2O2)МѕаЁЧвЦфГЬЖШДѓгкk2е§КЭc(O2)діДѓЕФГЬЖШЃЌЪЙШ§епЕФГЫЛ§МДv2е§МѕаЁ 6NO+3O2+2C2H4
ЃМ ЮТЖШЩ§ИпЃЌЗДгІЂйЁЂЂкЕФЦНКтОљФцвЦЃЌгЩгкЗДгІЂйЕФЫйТЪДѓЃЌЕМжТc(N2O2)МѕаЁЧвЦфГЬЖШДѓгкk2е§КЭc(O2)діДѓЕФГЬЖШЃЌЪЙШ§епЕФГЫЛ§МДv2е§МѕаЁ 6NO+3O2+2C2H4![]() 3N2+4CO2+4H2O 350ЁцЁЂИКдиТЪ3.0% 2Ni3+ + O2-Ёњ2Ni2+ +VO+
3N2+4CO2+4H2O 350ЁцЁЂИКдиТЪ3.0% 2Ni3+ + O2-Ёњ2Ni2+ +VO+![]() O2 NO + 6H+ +5e- = NH4+ + H2O
O2 NO + 6H+ +5e- = NH4+ + H2O
ЁОНтЮіЁПЃЈ1ЃЉЂй2NO(g)![]() N2O2(g)(Пь)ЃЌЂкN2O2(g)+ O2(g)
N2O2(g)(Пь)ЃЌЂкN2O2(g)+ O2(g) ![]() 2NO2(g)(Т§) ЃЌЛюЛЏФмдНДѓЃЌвЛАуЗжзгГЩЮЊЛюЛЏЗжзгдНФбЃЌЗДгІЫйТЪдНТ§ЃЌдђЗДгІЂйЕФЛюЛЏФмE1ЃМЗДгІЂкЕФЛюЛЏФмE2ЃЛЂй2NO(g)
2NO2(g)(Т§) ЃЌЛюЛЏФмдНДѓЃЌвЛАуЗжзгГЩЮЊЛюЛЏЗжзгдНФбЃЌЗДгІЫйТЪдНТ§ЃЌдђЗДгІЂйЕФЛюЛЏФмE1ЃМЗДгІЂкЕФЛюЛЏФмE2ЃЛЂй2NO(g)![]() N2O2(g)(Пь) ЁїH1<0ЃЌv1е§=k1е§c2(NO)ЃЌv1Фц=k1Фцc2(N2O2)ЃЌЂкN2O2(g)+ O2(g)
N2O2(g)(Пь) ЁїH1<0ЃЌv1е§=k1е§c2(NO)ЃЌv1Фц=k1Фцc2(N2O2)ЃЌЂкN2O2(g)+ O2(g) ![]() 2NO2(g)(Т§) ЁїH2<0ЃЌv2е§=k2е§c2(N2O2)c(O2)ЃЌv2Фц=k2Фцc2(NO2)ЃЌЖјФПБъЗДгІ2NOЃЈgЃЉ+O2ЃЈgЃЉ2NO2ЃЈgЃЉЕФЁїH=Ђй+Ђк=ЁїH1+ЁїH2ЃЌгЩЗДгІДяЦНКтзДЬЌЃЌЫљвдv1е§=v1ФцЁЂv2е§=v2ФцЃЌЫљвдv1е§ЁСv2е§=v1ФцЁСv2ФцЃЌМДk1е§c2ЃЈNOЃЉЁСk2е§cЃЈN2O2ЃЉcЃЈO2ЃЉ=k1ФцcЃЈN2O2ЃЉЁСk2Фцc2ЃЈNO2ЃЉЃЌдђK=
2NO2(g)(Т§) ЁїH2<0ЃЌv2е§=k2е§c2(N2O2)c(O2)ЃЌv2Фц=k2Фцc2(NO2)ЃЌЖјФПБъЗДгІ2NOЃЈgЃЉ+O2ЃЈgЃЉ2NO2ЃЈgЃЉЕФЁїH=Ђй+Ђк=ЁїH1+ЁїH2ЃЌгЩЗДгІДяЦНКтзДЬЌЃЌЫљвдv1е§=v1ФцЁЂv2е§=v2ФцЃЌЫљвдv1е§ЁСv2е§=v1ФцЁСv2ФцЃЌМДk1е§c2ЃЈNOЃЉЁСk2е§cЃЈN2O2ЃЉcЃЈO2ЃЉ=k1ФцcЃЈN2O2ЃЉЁСk2Фцc2ЃЈNO2ЃЉЃЌдђK= =
=![]() ЃЛИУЗДгІЮЊЗХШШЗДгІЃЌЮТЖШЩ§ИпЃЌЗДгІЂкЕФЦНКтФцвЦЃЌk2е§ЃМk2ФцЃЌМДaЃМbЃЛ2NO(g)+O2(g)
ЃЛИУЗДгІЮЊЗХШШЗДгІЃЌЮТЖШЩ§ИпЃЌЗДгІЂкЕФЦНКтФцвЦЃЌk2е§ЃМk2ФцЃЌМДaЃМbЃЛ2NO(g)+O2(g) ![]() 2NO2(g)ЮЊЗХШШЗДгІЃЌЮТЖШЩ§ИпЃЌЗДгІЂйЁЂЂкЕФЦНКтОљФцвЦЃЌгЩгкЗДгІЂйЕФЫйТЪДѓЃЌЕМжТc(N2O2)МѕаЁЧвЦфГЬЖШДѓгкk2е§КЭc(O2)діДѓЕФГЬЖШЃЌЪЙШ§епЕФГЫЛ§МДvspan>2е§МѕаЁЃЌЙЪД№АИЮЊЃКЃМЃЛЛюЛЏФмдНДѓЃЌвЛАуЗжзгГЩЮЊЛюЛЏЗжзгдНФбЃЌЗДгІЫйТЪдНТ§ЃЛ
2NO2(g)ЮЊЗХШШЗДгІЃЌЮТЖШЩ§ИпЃЌЗДгІЂйЁЂЂкЕФЦНКтОљФцвЦЃЌгЩгкЗДгІЂйЕФЫйТЪДѓЃЌЕМжТc(N2O2)МѕаЁЧвЦфГЬЖШДѓгкk2е§КЭc(O2)діДѓЕФГЬЖШЃЌЪЙШ§епЕФГЫЛ§МДvspan>2е§МѕаЁЃЌЙЪД№АИЮЊЃКЃМЃЛЛюЛЏФмдНДѓЃЌвЛАуЗжзгГЩЮЊЛюЛЏЗжзгдНФбЃЌЗДгІЫйТЪдНТ§ЃЛ ![]() ЃЛЃМЃЛЮТЖШЩ§ИпЃЌЗДгІЂйЁЂЂкЕФЦНКтОљФцвЦЃЌгЩгкЗДгІЂйЕФЫйТЪДѓЃЌЕМжТc(N2O2)МѕаЁЧвЦфГЬЖШДѓгкk2е§КЭc(O2)діДѓЕФГЬЖШЃЌЪЙШ§епЕФГЫЛ§МДv2е§МѕаЁЃЛ
ЃЛЃМЃЛЮТЖШЩ§ИпЃЌЗДгІЂйЁЂЂкЕФЦНКтОљФцвЦЃЌгЩгкЗДгІЂйЕФЫйТЪДѓЃЌЕМжТc(N2O2)МѕаЁЧвЦфГЬЖШДѓгкk2е§КЭc(O2)діДѓЕФГЬЖШЃЌЪЙШ§епЕФГЫЛ§МДv2е§МѕаЁЃЛ
ЃЈ2ЃЉЂйИљОнЭМЪОПЩжЊЃЌдкДпЛЏМСЕФзїгУЯТЃЌC2H4гыNOЁЂO2ЗДгІзюжеЩњГЩN2ЁЂCO2ЁЂH2OЃЌЗДгІжаn(NO):n(O2) =2ЃК1ЃЌЗДгІзмЗНГЬЪНЮЊ6NO+3O2+2C2H4![]() 3N2+4CO2+4H2OЃЌгЩЭМПЩжЊЃЌbЧњЯпЕФзюИпЕуДІЃЌЭбЯѕТЪИпЃЌИКдиТЪЕЭЃЌЪЪвЫЕФЮТЖШЃЌЪЪКЯЬѕМўЮЊ350ЁцЁЂИКдиТЪ3%ЃЌЙЪД№АИЮЊЃК6NO+3O2+2C2H4
3N2+4CO2+4H2OЃЌгЩЭМПЩжЊЃЌbЧњЯпЕФзюИпЕуДІЃЌЭбЯѕТЪИпЃЌИКдиТЪЕЭЃЌЪЪвЫЕФЮТЖШЃЌЪЪКЯЬѕМўЮЊ350ЁцЁЂИКдиТЪ3%ЃЌЙЪД№АИЮЊЃК6NO+3O2+2C2H4![]() 3N2+4CO2+4H2OЃЛ350ЁцЁЂИКдиТЪ3.0%ЃЛ
3N2+4CO2+4H2OЃЛ350ЁцЁЂИКдиТЪ3.0%ЃЛ
ЂкгУNOПЩжБНгДпЛЏNOЗжНтЩњГЩN2ЁЂO2ЃЌЗДгІЕФзмЗДгІЮЊ2NO![]() O2+N2ЃЌИљОнЗДгІдРэЃЌNi2+ЮЊДпЛЏМСЃЌгУзмЗДгІ-ЃЈ2Ni2++2Vo+2NOЁњ2Ni3++2O-+N2ЃЉ-ЃЈ2O-Ёњ+O2-+1/2O2+Vo)ЕУЃК2Ni3+ + O2-Ёњ2Ni2+ +VO+
O2+N2ЃЌИљОнЗДгІдРэЃЌNi2+ЮЊДпЛЏМСЃЌгУзмЗДгІ-ЃЈ2Ni2++2Vo+2NOЁњ2Ni3++2O-+N2ЃЉ-ЃЈ2O-Ёњ+O2-+1/2O2+Vo)ЕУЃК2Ni3+ + O2-Ёњ2Ni2+ +VO+![]() O2ЃЌЙЪД№АИЮЊЃК2Ni3+ + O2-Ёњ2Ni2+ +VO+
O2ЃЌЙЪД№АИЮЊЃК2Ni3+ + O2-Ёњ2Ni2+ +VO+![]() O2ЃЛ
O2ЃЛ
ЃЈ3ЃЉЕчНтNOжЦБИNH4NO3ЃЌбєМЋЗДгІЮЊNO-3e-+2H2O=NO3-+4H+ЃЌвѕМЋЗДгІЮЊЃКNO+5e-+6H+=NH4++H2OЃЌЙЪД№АИЮЊЃКNO + 6H+ +5e- = NH4+ + H2OЁЃ

ЁОЬтФПЁПгУЯТСазАжУжЦБИЖўбѕЛЏЕЊЦјЬх,ВЂЬНОПЯрЙиВњЮяаджЪЁЃ
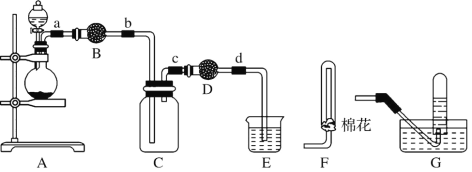
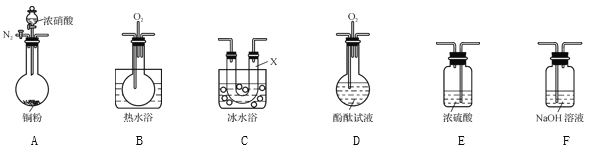
(1) зАжУAжаЕФЗжвКТЉЖЗЪЂзАЕФвКЬхЪЧ____,ЩеЦПжадЄЯШМгШыЕФЪЧЭаМ,ЬњЕФМлИёБШЭЕФМлИёЕЭ,ДЫДІгУЭВЛгУЬњЕФдвђЪЧ______________ЁЃ
(2) ИЩдяЙмBЁЂDжаЪЂзАЕФИЩдяМСПЩвдЪЧ____(ЬюЁАХЈСђЫсЁБЁЂЁАЮоЫЎТШЛЏИЦЁБЁЂЁАЮхбѕЛЏЖўСзЁБЛђЁАМюЪЏЛвЁБ),ИЩдяЙмDжаИЩдяМСЕФзїгУЪЧ______________ЁЃ
(3) зАжУEЕФзїгУЪЧЮќЪеЮВЦј,ЮќЪеЙ§ГЬжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНШчЯТ,ЧыНЋЦфВЙГфЭъећЁЃ
NaOH+ NO2![]() ЁЁЁЁЁЁ+ NaNO2+ H2O ______
ЁЁЁЁЁЁ+ NaNO2+ H2O ______
(4) ФГЛЏбЇаЫШЄаЁзщШЯЮЊЭКЭЪЪСПХЈЯѕЫсЗДгІВњЩњЕФЦјЬхжаКЌNO,бЁгУЯТСаБивЊЕФзАжУ(N2КЭO2ЕФгУСППЩздгЩПижЦ)ЭъГЩбщжЄЪЕбщЁЃ
вбжЊ:
i. NO+NO2+2OH-![]() 2NO2-+H2O
2NO2-+H2O
iiЦјЬхвКЛЏЮТЖШШчЯТ:
ЦјЬх | NO2 | NO |
вКЛЏЮТЖШ | 21 Ёц | -152 Ёц |
ЂйвЧЦїЕФСЌНгЫГађ(АДДгзѓЁњгвСЌНг,ЬюИївЧЦїзжФИ)ЮЊ________ЁЃ
ЂкЪЕбщЪБЯШМьВщзАжУЦјУмадКѓ,дйМгШыЪдМС,дкЗДгІЧАЕФВйзїЪЧ_______ЁЃ
ЂлШЗШЯЦјЬхжаКЌNOЕФЯжЯѓЪЧ__________;зАжУCЕФзїгУЪЧ____ЁЃ
ЂмNH3ДпЛЏЛЙдЕЊбѕЛЏЮя(SCR)ММЪѕЪЧФПЧАгІгУзюЙуЗКЕФЦјЬхжаЕЊбѕЛЏЮяЭбГ§ММЪѕЁЃЯждкгаNOЁЂNO2ЕФЛьКЯЦј6 L,ПЩгУЭЌЮТЭЌбЙЯТ7 L NH3ЧЁКУЪЙЦфЭъШЋзЊЛЏЮЊN2,дђдЛьКЯЦјЬхжаNOКЭNO2ЕФЮяжЪЕФСПжЎБШЮЊ____ЁЃ
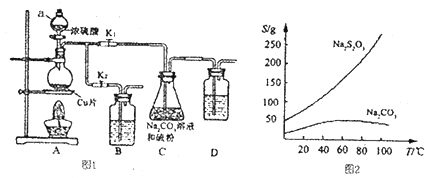
ЁОЬтФПЁПютЪЧвЛжжживЊЕФЙ§ЖЩН№ЪєдЊЫиЃЌЭЈГЃгУзїКЯН№МАВЛатИжЕФЬэМгМСЃЌПЩдіЧПКЯН№ЕФЧПЖШЁЂгВЖШЁЂПЩКИадЕШЁЃютЫсФЦОЇЬх(Na2MoO4ЁЄ2H2O)ПЩзїЮЊЮоЙЋКІаЭРфШДЫЎЯЕЭГЕФН№ЪєИЏЪДвжжЦМСЃЌШчЭМ15ЪЧЛЏЙЄЩњВњжавдЛдютПѓ(жївЊГЩЗжЮЊСђЛЏютMoS2)ЮЊдСЯРДжЦБИН№ЪєютЁЂютЫсФЦОЇЬхЕФжївЊСїГЬЭМЁЃ
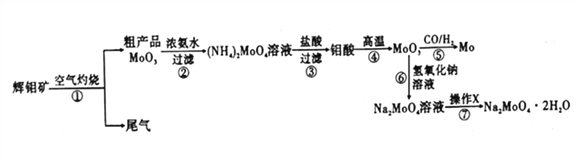
ЛиД№ЯТСаЮЪЬт:
ЃЈ1ЃЉвбжЊЗДгІЂлЮЊИДЗжНтЗДгІЃЌдђютЫсжадПЕФЛЏКЯМлЮЊ___________ЁЃ
ЃЈ2ЃЉЗДгІЂоЕФРызгЗНГЬЪНЮЊ___________ЁЃ
ЃЈ3ЃЉЛдютПѓзЦЩеЪБЕФЛЏбЇЗНГЬЪНЮЊ____________ЁЃ
ЃЈ4ЃЉВйзїXЮЊ_________ЁЃвбжЊютЫсФЦдквЛЖЈЮТЖШЗЖЮЇФкЕФЮіГіЮяжЪМАЯргІЮяжЪЕФШмНтЖШШчЯТБэЫљЪОЃЌдђдкВйзїXжагІПижЦЮТЖШЕФзюМбЗЖЮЇЮЊ_______(ЬюађКХ)ЁЃ
ЮТЖШ(Ёц) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 | >100 |
ЮіГіЮяжЪ | Na2MoO4ЁЄ10H2O | Na2MoO4ЁЄ2H2O | Na2MoO4 | ||||||
ШмНтЖШ | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45.57 | |
A.0ЁцЁЋ10Ёц B.10ЁцЁЋ100Ёц C.15.5ЁцЁЋ50Ёц D.100ЁцвдЩЯ
ЃЈ5ЃЉжЦБИютЫсФЦОЇЬхЛЙПЩгУЭЈЙ§ЯђОЋжЦЕФЛдютПѓжажБНгМгШыДЮТШЫсФЦШмвКбѕЛЏЕФЗНЗЈЃЌШєбѕЛЏЙ§ГЬжаЃЌЛЙгаСђЫсФЦЩњГЩЃЌдђбѕЛЏМСгыЛЙдМСЕФЮяжЪЕФСПжЎБШЮЊ_________ЁЃ
ЃЈ6ЃЉLiЁЂMoS2ПЩГфЕчЕчГиЕФЙЄзїдРэЮЊxLi+nMoS2![]() Lix(MoS2)n[Lix(MoS2)nИНзХдкЕчМЋЩЯ]ЃЌдђЕчГиГфЕчЪБбєМЋЕФЕчМЋЗДгІЪНЮЊ___________________ЁЃ
Lix(MoS2)n[Lix(MoS2)nИНзХдкЕчМЋЩЯ]ЃЌдђЕчГиГфЕчЪБбєМЋЕФЕчМЋЗДгІЪНЮЊ___________________ЁЃ
ЃЈ7ЃЉПЩгУЛЙдадЦјЬх(COКЭH2)ЛЙдMoO3жЦютЃЌвЕЩЯжЦБИЛЙдадЦјЬхCOКЭH2ЕФЗДгІдРэжЎвЛЮЊCO2+CH4![]() 2CO+2H2ЁЃКЌМзЭщЬхЛ§ЗжЪ§ЮЊ90%ЕФ7L(БъзМзДПі)ЬьШЛЦјгызуСПЖўбѕЛЏЬМдкИпЮТЯТЗДгІЃЌМзЭщзЊЛЏТЪЮЊ80%,гУВњЩњЕФCOКЭH2ЛЙдMoO3жЦютЃЌРэТлЩЯФмЩњВњютЕФжЪСПЮЊ_________ЁЃ
2CO+2H2ЁЃКЌМзЭщЬхЛ§ЗжЪ§ЮЊ90%ЕФ7L(БъзМзДПі)ЬьШЛЦјгызуСПЖўбѕЛЏЬМдкИпЮТЯТЗДгІЃЌМзЭщзЊЛЏТЪЮЊ80%,гУВњЩњЕФCOКЭH2ЛЙдMoO3жЦютЃЌРэТлЩЯФмЩњВњютЕФжЪСПЮЊ_________ЁЃ